
 Si+2CO↑,在反应中SiO2发生了______(填“氧化”或“还原”)反应.该反应生产的是粗硅,将粗硅提纯才能得到高纯硅,在提纯过程中发生的反应之一是:H2+SiCl4
Si+2CO↑,在反应中SiO2发生了______(填“氧化”或“还原”)反应.该反应生产的是粗硅,将粗硅提纯才能得到高纯硅,在提纯过程中发生的反应之一是:H2+SiCl4 HCl+X,X的化学式为______.
HCl+X,X的化学式为______. Si+2CO↑中,SiO2失去氧而生成单质Si,发生失氧的还原反应;
Si+2CO↑中,SiO2失去氧而生成单质Si,发生失氧的还原反应; HCl+X,反应前的两种反应物的分子中含H、Si、Cl三种原子的个数分别为2、1、4,而生成物HCl的一个分子由仅含有1个H原子和1个Cl原子,根据反应前后原子种类、数目不变,可判断生成的每个X分子由1个H原子、1个Si原子和3个Cl原子构成,则物质X的化学式为HSiCl3;
HCl+X,反应前的两种反应物的分子中含H、Si、Cl三种原子的个数分别为2、1、4,而生成物HCl的一个分子由仅含有1个H原子和1个Cl原子,根据反应前后原子种类、数目不变,可判断生成的每个X分子由1个H原子、1个Si原子和3个Cl原子构成,则物质X的化学式为HSiCl3; 2NaOH+Cl2↑+H2↑;氢气在氯气中燃烧生成的氯化氢气体极易溶于水,与空气中的水蒸气结合成盐酸的小液滴而形成“白雾”;
2NaOH+Cl2↑+H2↑;氢气在氯气中燃烧生成的氯化氢气体极易溶于水,与空气中的水蒸气结合成盐酸的小液滴而形成“白雾”; 2NaOH+Cl2↑+H2↑;盐酸液滴.
2NaOH+Cl2↑+H2↑;盐酸液滴.

 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:初中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:重庆 题型:填空题
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:2011-2012学年重庆市全善学校九年级(下)第二次月考化学试卷(解析版) 题型:填空题
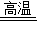 Si+2CO↑,在反应中SiO2发生了 (填“氧化”或“还原”)反应.该反应生产的是粗硅,将粗硅提纯才能得到高纯硅,在提纯过程中发生的反应之一是:H2+SiCl4
Si+2CO↑,在反应中SiO2发生了 (填“氧化”或“还原”)反应.该反应生产的是粗硅,将粗硅提纯才能得到高纯硅,在提纯过程中发生的反应之一是:H2+SiCl4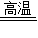 HCl+X,X的化学式为 .
HCl+X,X的化学式为 .查看答案和解析>>
科目:初中化学 来源:2011年重庆市垫江县包家学校中考化学模拟试卷(解析版) 题型:填空题
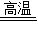 Si+2CO↑,在反应中SiO2发生了 (填“氧化”或“还原”)反应.该反应生产的是粗硅,将粗硅提纯才能得到高纯硅,在提纯过程中发生的反应之一是:H2+SiCl4
Si+2CO↑,在反应中SiO2发生了 (填“氧化”或“还原”)反应.该反应生产的是粗硅,将粗硅提纯才能得到高纯硅,在提纯过程中发生的反应之一是:H2+SiCl4 HCl+X,X的化学式为 .
HCl+X,X的化学式为 .查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com