
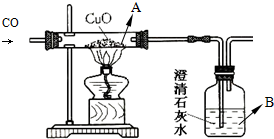
| ||
| ||
| ||
| mCu |
| mO |
| 64 |
| 16 |
| X |
| 1.6g |
| ||
| 64 |
| 44 |
| X |
| 4.4g |


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
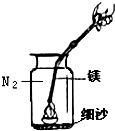 林林做镁带在空气中燃烧实验时,发现生成的白色固体的质量小于参加反应的金属镁和氧气的质量和.他在一本参考书上发现,镁居然能在氮气中燃烧!于是他做起了这个实验:将镁条点燃后迅速伸入盛有氮气的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种叫氮化镁(Mg3N2)的粉末.
林林做镁带在空气中燃烧实验时,发现生成的白色固体的质量小于参加反应的金属镁和氧气的质量和.他在一本参考书上发现,镁居然能在氮气中燃烧!于是他做起了这个实验:将镁条点燃后迅速伸入盛有氮气的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种叫氮化镁(Mg3N2)的粉末.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
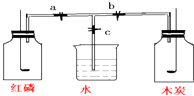 关闭止水夹a、b、c,使过量的红磷和木炭分别在盛有空气的等容积的甲、乙两瓶中同时燃烧,如图所示,试回答:
关闭止水夹a、b、c,使过量的红磷和木炭分别在盛有空气的等容积的甲、乙两瓶中同时燃烧,如图所示,试回答:查看答案和解析>>
科目:初中化学 来源: 题型:
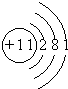 下图是元素周期表的一部分,据此回答下列问题:
下图是元素周期表的一部分,据此回答下列问题:| 第二周期 | 3Li 锂 7 | 4Be 铍 9 | 5B 硼 11 | ① | 7 N 氮 14 | 8 O 氧 16 | 9 F 氟 19 | 10 Ne 氖 20 |
| 第三周期 | ② | 12 Mg 镁 | 13 Al 铝 27 | 14 Si 硅 28 | ③ | 16 S 硫 32 | 17 Cl 氯 35.5 | 18 Ar 氩 40 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com