
| 实验步骤 | ①称烧杯的质量 | ②将适量稀盐酸加入烧杯中并称重 | ③称取少量大理石样品,并加入②的烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验数据 | 烧杯的质量为50.0g | 烧杯和稀盐酸的质量为l00.0g | 大理石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
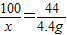
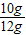 ×100%≈83.3%
×100%≈83.3%

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:初中化学 来源: 题型:
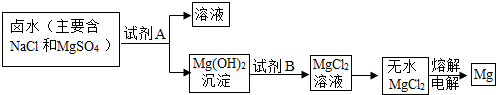
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | ①称烧杯的质量 | ②将适量稀盐酸加入烧杯中并称重 | ③称取少量大理石样品,并加入②的烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验数据 | 烧杯的质量为50.0g | 烧杯和稀盐酸的质量为l00.0g | 大理石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | ①称烧杯的质量 | ②将适量稀盐酸加入烧杯中并称重 | ③称取少量大理石样品,并加入②的烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验数据 | 烧杯的质量为50.0g | 烧杯和稀盐酸的质量为l00.0g | 大理石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
查看答案和解析>>
科目:初中化学 来源:张家界 题型:问答题
| 实验步骤 | ①称烧杯的质量 | ②将适量稀盐酸加入烧杯中并称重 | ③称取少量大理石样品,并加入②的烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验数据 | 烧杯的质量为50.0g | 烧杯和稀盐酸的质量为l00.0g | 大理石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com