
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
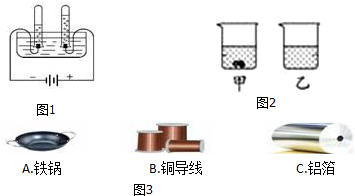
分析 (1)根据电解水的反应,写出反应的化学方程.
(2)①根据在40℃时,KNO3和KCl溶解度的大小分析;
②根据饱和溶液与不饱和溶液之间的转化关系分析;
(3)根据金属的应用分析金属的性质;
(4)根据铁生锈的条件和防止生锈的措施分析回答;
(5)根据氧化铁、铁与盐酸的反应写出反应的方程式;
(6)根据金属活动性顺序,位置在前的金属能将后面的金属从其盐溶液中置换出来分析.
解答 解:(1)由图1可知电解水生成了氢气和氧气,此反应的方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(2)①由溶解度可知,在40℃时,KNO3的溶解度是63.9g,KCl的溶解度是40.0g,由乙烧杯的溶质全部溶解了,说明了乙烧杯中的溶质是KNO3;
②A、当升高温度时,烧杯中的剩余固体全部溶解,溶液变为不饱和溶液,溶剂质量不变.故A说法正确;
B.当加入溶剂时,烧杯中的剩余固体全部溶解,溶液变为不饱和溶液,溶液中溶质的质量分数不一定增大.故B说法错误;
C.可采用升温的方法使溶质溶解了,溶液质量不一定增大.故C说法错误;
D.可采用升温或加水的方法,都可以使烧杯中的剩余固体全部溶解,溶液变为不饱和溶液,故D说法正确;
(3)利用铁锅做饭,主要利用铁具有良好导热性,故选A;
(4)铁制品在空气中会发生锈蚀,其原因是铁与空气中的氧气和水共同作用的结果.为防止钢铁制品的锈蚀,厨房中的铁锅和菜刀通常需做的防护是 擦干或涂油.
(5)在探究金属的化学性质时,某同学将带锈铁钉放入稀盐酸中,观察到铁锈逐渐消失,溶液由无色逐渐变成黄色,并有气泡产生,有关反应的化学方程式为 Fe2O3+6HCl=2FeCl3+3H2O,Fe+2HCl=FeCl2+H2↑.
(6)由于金属的活动性是大小是镁>铁>铜,向含有FeSO4和CuSO4两种溶质的溶液中,加入一定质量镁粉,镁首先与硫酸铜反应,当硫酸铜反应完成后,再与硫酸亚铁反应,由于滤液呈浅绿色,说明了镁全部参加了反应.由此可知:
A.滤纸上一定有Cu,可能有Fe,一定没有Mg.故A说法正确;
B.滤纸上不一定有Fe,一定没有Mg,一定有铜Cu.故B说法错误;
C.滤液中一定有MgSO4.故C说法错误;
D.滤液中一定有MgSO4、FeSO4,一定没有CuSO4.故D说法正确.
故答为:(1)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑; (2)①KNO3,②A、D,(3)A;(4)氧气和水 擦干或涂油
(5)Fe2O3+6HCl=2FeCl3+3H2O,Fe+2HCl=FeCl2+H2↑;(6)A、D.
点评 本题比较全面考查了金属材料和水的知识,金属材料和水的在生产和生活中有着广泛应用,应加强有关知识的学习.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:初中化学 来源:山东省临沂市蒙阴县2017届九年级第二轮模拟考试化学试卷 题型:信息分析题
甲、乙两种固体物质的溶解度曲线如图所示,据图回答下列问题:

(1)甲物质的溶解度随温度的升高而____(填“增大”或“减小”);
(2)30℃时,将40g甲物质加入到100g水中充分溶解后,所得溶液的质量为__________g;
(3)若甲物质中混有少量乙物质,可用______的方法提纯甲;
(4)等质量甲、乙两种物质分别配成30℃时的饱和溶液,需要水的质量大小关系是甲____乙(填“>”、“=”或“<”)。
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
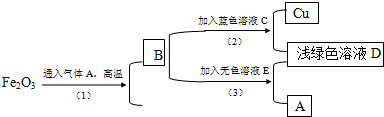
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 计算需氯化钠3g、水47g | |
| B. | 将氯化钠固体放于纸上称量 | |
| C. | 将氯化钠固体放入量筒中溶解 | |
| D. | 将配好的氯化钠溶液装瓶并贴好标签 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
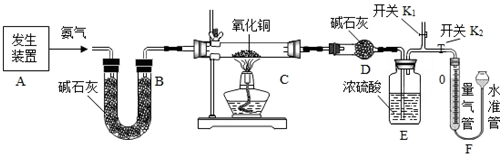
查看答案和解析>>
科目:初中化学 来源:山东省临沂市蒙阴县2017届九年级第二轮模拟考试化学试卷 题型:信息分析题
化学课上我们曾经观察过如图所示的实验。
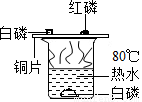
(1)实验中,铜片上的白磷很快燃烧,其反应的化学方程式为______________;
(2)该实验主要利用了铜片良好的______性,燃着的白磷熄灭后,去掉铜片上的白色固体,可看到铜片表面变黑,该黑色物质是______(填化学式);
(3)烧杯中的水在实验中没有起到的作用是___(填序号)。
A.作反应物 B.隔绝空气 C.升高温度
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
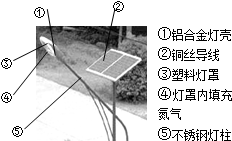 随着科技的不断进步,太阳能路灯(如图所示)越来越多的出现在我们城市道路的两旁.节约能源的同时减少了环境的污染,是实现“低碳生活”的一种典型措施.请你根据图中内容回答下列问题:
随着科技的不断进步,太阳能路灯(如图所示)越来越多的出现在我们城市道路的两旁.节约能源的同时减少了环境的污染,是实现“低碳生活”的一种典型措施.请你根据图中内容回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com