
【题目】用NA表示阿伏伽德罗常数的值。下列叙述中正确的是( )
A. 分子总数为NA 的NO2和CO2混合气体中含有的氧原子数为4NA
B. 常温常压下,92gNO2和N2O4混合气体中含有的原子数为6NA
C. 1mol SO3中含有的分子数目为4NA
D. 含有3.01×1023个原子的氮气中,N2的分子数为0.5NA
【答案】B
【解析】
A. 分子总数为 NA 的 NO2 和 CO2 混合气体中含有的氧原子数为2NA,因为不管是NO2还是CO2一个分子只有2个氧原子,而分子总数是NA个,故氧原子数为2NA,故不符合题意;
B. 常温常压下,92gNO2 和 N2O4 混合气体中含有的原子数为 6NA,说法正确,因为NO2 和 N2O4 的N、O原子个数比为1:2,其摩尔质量为![]() ,其物质的量为
,其物质的量为![]() ,1mol有3NA个原子,2mol有6NA个原子,故符合题意;
,1mol有3NA个原子,2mol有6NA个原子,故符合题意;
C. 1molSO3 中含有的分子数目为NA,含有的原子数为4NA。故不符合题意;
D. 含有 3.01×1023 个原子的氮气,有0.25mol的氮气,N2 的分子数为 0.25NA。故不符合题意;


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:
【题目】如图所示为A、B、C三种固体物质的溶解度曲线,下列有关说法正确的是(_______)
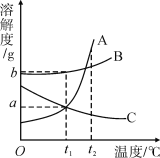
A.t2 ℃时三种物质的饱和溶液中,溶质质量最大的是A
B.将t1 ℃时,A、B、C三种物质的饱和溶液,分别蒸发等量的水后温度恢复至t1 ℃,析出溶质的质量关系为B>A=C
C.可用降低温度的方法使t2 ℃时C的不饱和溶液变为饱和溶液
D.将t2 ℃时三种物质的饱和溶液降温至t1 ℃时,溶质的质量分数由大到小的顺序是______________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】 资料一: “见著知微”是化学学习者应该具备的基本素养,也是学习化学的重要思想方法。
资料二:氟及其化合物常运用于原子弹制造、航天工业等领域。氟气(F2)化学性质极其活泼,水都能在氟气中燃烧,且燃烧产物是氧气。结合以上信息,回答下列问题:
(1)氮原子核外有_____个电子层,如图B中x=_____,在氟元素形成的化合物中,氟元素通常显_____价。

(2)如图是水与氟气反应的微观示意图。如图方框内应填如图中的_____选项,选择此选项的理由是_____________________________。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】市售塑料袋有的是用聚乙烯[(CH2CH2)n]制成,有的是用聚氯乙烯[(CH2CHCl)n]制成,通过查阅资料可知:(CH2CHCl)n+![]() O2
O2![]() 2nCO2+nH2O+nHCl,其中n是上千或上万的数值;HCl气体极易溶于水,有刺鼻气味,其水溶液即是盐酸;鉴别盐酸的方法是加入AgNO3溶液,观察是否产生白色沉淀.
2nCO2+nH2O+nHCl,其中n是上千或上万的数值;HCl气体极易溶于水,有刺鼻气味,其水溶液即是盐酸;鉴别盐酸的方法是加入AgNO3溶液,观察是否产生白色沉淀.
①通过点燃的方法可以鉴别聚乙烯和聚氯乙烯.如果塑料袋点燃时有强烈的刺鼻气味,这种塑料袋可能是由________制成的.
②某同学设计了如下图所示实验来探究塑料燃烧的产物.
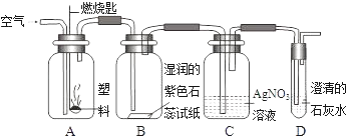
若A瓶燃烧的是聚氯乙烯塑料,在B瓶中可以看到的现象是________,C、D两瓶中发出反应的化学方程式为________、________;
若A瓶中用的是聚乙烯塑料,则在C瓶中能观察到的现象是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据实验回答下列问题:
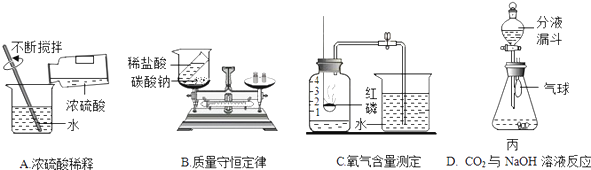
(1)A实验中的操作是:________,其中玻璃棒不断搅拌的作用是________.
(2)B实验中设计不合理的原因是________,是否符合质量守恒定律________.
(3)C实验中测得氧气含量偏大的原因可能是________(答出一点即可).
(4)D实验分液漏斗里是NaOH溶液锥形瓶中是CO2,将NaOH溶液滴入锥形瓶中,其发生反应的方程式为________,当同学发现气球涨大认为反应发生,但桐桐认为还应该补充的对比实验是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学研究性学习小组同学取 10g 石灰石样品,用足量的稀盐酸测定石灰石中碳酸钙的质量分数(假设石灰石中杂质不与盐酸反应)。测量 5 分钟内生成 CO2 质量的数据如下表:
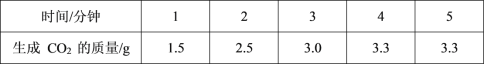
请回答下列问题:
I.石灰石中的 CaCO3 完全反应时,生成二氧化碳气体的物质的量为_____mol。
II.该石灰石中 CaCO3 的质量分数是多少_______?(根据化学方程式列式计算)
III.请根据表中数据分析,你能发现数据背后的化学反应规律是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
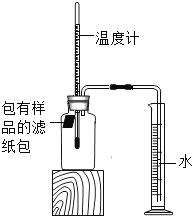
【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表。
序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
1 | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
3 | …… | 100 | 70 | 约480 |
(1)实验①和②说明NaCl可以_____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是_____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是_____。
(4)已知含碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成_____。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是_____(小数点后保留1位)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:

(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称 ;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是 ;
(2)用PH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”“中性”或“碱性”)溶液,白醋pH (填“>””<”或”=”)7;
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 (填“A”“B”或“C”,下同),可能导致北侧溶液pH数值发生改变的错误操作是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com