
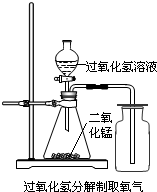
 实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.分析 (1)用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成;过氧化氢溶液在二氧化锰催化作用下生成水和氧气去分析;
(2)根据O2的密度比空气密度略大去分析;
(3)由氧气的验满方法去分析;
(4)过氧化氢溶液的浓度越大,反应速率越快,因此要想降低反应速率就要降低过氧化氢溶液的浓度;可换用体积较大的锥形瓶,防止由于反应速度过快,产生气体过多导致锥形瓶爆炸;
(5)根据过氧化氢制氧气的装置和高锰酸钾制取氧气的装置图的比较考虑,再根据制取相同质量的氧气需要它们的价格考虑.
解答 解:(1)用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,所以化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
过氧化氢溶液在二氧化锰催化作用下生成水和氧气,二氧化锰在反应前后质量和化学性质都没有改变,只是加快了过氧化氢反应生成氧气的速率,故二氧化锰是催化剂,所以二氧化锰就应该作为反应条件写在等号的上方,故化学方程式为:2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑;
故答案为:2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑ 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)由于O2的密度比空气密度略大所以可用向上排空气法收集;故答案为:向上排空气法 氧气的密度比空气大;
(3)由于氧气的密度比空气大,进入集气瓶后,沉积在集气瓶的底部,氧气自下而上,充满集气瓶,当瓶口有氧气时,说明氧气已收集满,检验氧气是否集满的方法是利用氧气的助燃性,用带火星的木条放在集气瓶口,如果复燃,证明集气瓶内已充满氧气;故答案为:C;
(4)过氧化氢溶液的浓度越大,反应速率越快,因此要想降低反应速率就要降低过氧化氢溶液的浓度;可换用体积较大的锥形瓶,防止由于反应速度过快,产生气体过多导致锥形瓶爆炸,故答案为:①②;
(5)由于过氧化氢分解制取氧气不需要加热,所以操作简单安全;
设要制取3.2g氧气需要高锰酸钾质量为x,需要过氧化氢质量为y
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 3.2g
根据:$\frac{316}{32}=\frac{x}{3.2g}$
解得x=31.6g
需要过氧化氢质量为y,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
y 3.2g
根据:$\frac{68}{32}=\frac{y}{3.2g}$
解得y=6.8g,所以需质量分数为30%过氧化氢溶液的质量为:$\frac{6.8g}{30%}$=22.7g;
则制取3.2g氧气如果用高锰酸钾需要花费31.6g×0.0305元/g=0.9638元;如果用过氧化氢溶液则花费22.7g×0.0217元/g=0.49259元;可以知道:制取相同质量O2时购买H2O2比KMnO4价格低;
故答案为:操作简单安全 制取相同质量O2时购买H2O2比KMnO4价格低.
点评 题目综合考查了氧气的实验室制法,特别是最后一问,根据化学反应方程式的计算的审题是非常关键的,一般是抓住“三找”;即一找化学反应方程式,二找已知量和未知量x,三找用到的相对质量关系,同时注意解题步骤和格式.


 综合自测系列答案
综合自测系列答案科目:初中化学 来源: 题型:选择题
| A. | 2O3C | B. | O2C3 | C. | C2O3 | D. | C3O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 被测植物 | 平均伤斑面积(%) |
| 甲 | 13.5 |
| 乙 | 33.4 |
| 丙 | 57.7 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
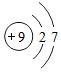 ,下列说法错误的是( )
,下列说法错误的是( )| A. | 氟原子的核内质子数为9 | B. | 氟原子核外有2个电子层 | ||
| C. | 氟原子的核内中子数为9 | D. | 氟原子的核电荷数为9 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 西瓜汁(pH:5.5~6) | B. | 柠檬汁 (pH:2.2~3) | ||
| C. | 酱油(pH:4.3~5) | D. | 厕所清洁剂(pH:1.2~2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com