
| 物质 | 所含杂质 | 方法 | |
| A | N2 | O2 | 通过灼热的铜丝 |
| B | CaO | CaCO3 | 加入适量的稀盐酸 |
| C | CO2 | HCl | 通过足量的氢氧化钠溶液 |
| D | NaCl溶液 | Na2CO3 | 加入适量的Ca(NO3)2溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、氧气通过灼热的铜丝时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、CaO和CaCO3均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、Na2CO3能与适量的Ca(NO3)2溶液反应生成碳酸钙沉淀和硝酸钠,能除去杂质但引入了新的杂质硝酸钠,不符合除杂原则,故选项所采取的方法错误.
故选:A.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 据质量守恒定律,5g氢气和5g氧气混合点燃充分反应生成水的质量一定是10g | |
| B. | 蒸发20g食盐水后得到2g食盐和18g水,符合质量守恒定律 | |
| C. | 参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和 | |
| D. | 镁条在空气中燃烧后,生成物质量比镁条的质量增加了,这违背了质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 事 实 | 解 释 | |
| A | 铁器比铝器更易生锈 | 铁比铝更活泼 |
| B | 金鱼在冷开水中死亡 | 冷开水中不含氧元素 |
| C | 打开可乐瓶盖冒出大量气泡 | 气体的溶解度随压强的减小而减小 |
| D | 餐具上的油污可用洗洁精洗去 | 洗洁精能够溶解油污 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
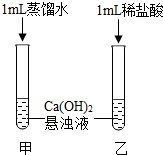 同学们对氢氧化钙的性质进行探究.
同学们对氢氧化钙的性质进行探究.| 实验操作 | 实验现象 | 结论 |
| 向乙试管内的液体中滴加石蕊试液(或碳酸氢钠溶液等); | 溶液显红色(或有气泡产生等). | 猜想②成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将河水经过沉淀、过滤、活性炭吸附等净化处理后,所得的水就是纯水 | |
| B. | 按质量计算,空气中约含氮气78%、氧气21%、稀有气体等其他成分1% | |
| C. | 洗涤剂能洗涤餐具上油污的原因是洗涤剂可以使油脂乳化 | |
| D. | 实验室中含有盐酸的废水可以直接倒入下水道(铸铁管道) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 称取NaCl和BaCl2的固体混合物32.5g,加入148.8g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:
称取NaCl和BaCl2的固体混合物32.5g,加入148.8g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
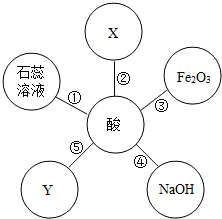 硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如下图体现了酸类物质的化学性质,其中X、Y及图中所给其他物质的类别不同.结合此图回答下列问题.
硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如下图体现了酸类物质的化学性质,其中X、Y及图中所给其他物质的类别不同.结合此图回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com