
 14、NaNO2、NaCl和物质M的溶解度曲线如图1所示.当往试管中加入5mL稀盐酸时,图2烧杯中饱和溶液变浑浊,下列说法正确的是( )
14、NaNO2、NaCl和物质M的溶解度曲线如图1所示.当往试管中加入5mL稀盐酸时,图2烧杯中饱和溶液变浑浊,下列说法正确的是( )

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:
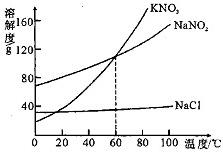 22、KNO3、NaNO2、NaCl三种固体物质的溶解度曲线如右图所示,回答下列问题:
22、KNO3、NaNO2、NaCl三种固体物质的溶解度曲线如右图所示,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
工业用盐中常混有亚硝酸钠(NaNO2),NaNO2外观酷似食盐且有咸味,生活中易发生亚硝酸钠中毒事件.有关NaNO2和NaCl的部分资料如下表:
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com