
| A. | 浓盐酸变稀与空气中水蒸气有关 | |
| B. | 氢氧化钠溶液变质与空气中二氧化碳有关 | |
| C. | 氧化钙的变质与空气中的水和二氧化碳有关 | |
| D. | 铁生锈与空气中的水蒸气、氧气有关 |
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  ZnSO4溶液 | B. | 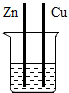 FeSO4溶液 | ||
| C. |  ZnSO4溶液 CuSO4溶液 | D. | 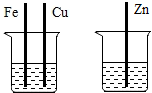 稀盐酸 FeSO4溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 教科书循环使用 | |
| B. | 多用电子邮箱、QQ等即时通讯工具 | |
| C. | 禁止使用煤、石油、天然气 | |
| D. | 提倡乘坐公共交通工具、骑自行车或步行等出行方式 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 焚烧垃圾发电 | B. | 焚烧大量秸杆 | ||
| C. | 用旧报纸制铅笔杆 | D. | 使用可降解塑料 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
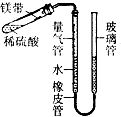 某课外活动小组的同学用如图所示装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是:
某课外活动小组的同学用如图所示装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com