

| 蒸发皿的质量 | 蒸发皿的质量+ 食盐溶液的质量 |
蒸发皿的质量+ 食盐晶体的质量 |
| 28.8g | 48.8g | 30.7g |
| 1.9g |
| 20g |
| 58.5 |
| 170 |
| X |
| 34.2g×17% |
| 2.0g |
| 20g |


 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:初中化学 来源: 题型:
 13、学校化学兴趣小组进行探究性学习,同学们设计如右图所示装置进行一系列的实验;
13、学校化学兴趣小组进行探究性学习,同学们设计如右图所示装置进行一系列的实验;查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验步骤 | 现象 | 结论 | |
| 甲 | 加入5ml的蒸馏水, 振荡使之充分混合 |
试管中的硝酸接近于无色 | 硝酸中没有其它杂质,猜想正确 |
| 乙 | 置于酒精灯上小火加热(在通风厨中进行) | 有红棕色气体逸出,继续加热,直到不再有红棕色气体逸出为止.溶液的黄色变浅,但不能完全消失. | 呈黄色的工业硝酸中存在NO2气体,但还有其它呈黄色物质 . |
| 丙 | 通入氧气 | 通入足量氧气后,溶液的黄色变浅. |
| 实验步骤 | 现象 | 结论 | |
| 乙 | 在除去NO2的工业硝酸中,缓缓加入足量NaOH固体 | 产生红褐色沉淀 |
猜想 正确 |
| 丙 | 在除去NO2的工业硝酸中加入硫氰化钾 | 产生血红色物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:
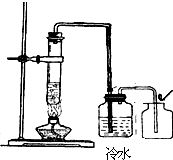 某学校化学兴趣小组同学在学习了制取氧气这~节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是
某学校化学兴趣小组同学在学习了制取氧气这~节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是查看答案和解析>>
科目:初中化学 来源: 题型:
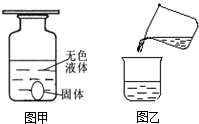 某学校化学兴趣小组在化学实验室做实验时,甲班的王明同学把一种白色固体和一种无色液体混合,发现固体溶解时放出热量但没有气体放出.乙班的张正同学把两种无色液体混合时,也出现了同样的现象.
某学校化学兴趣小组在化学实验室做实验时,甲班的王明同学把一种白色固体和一种无色液体混合,发现固体溶解时放出热量但没有气体放出.乙班的张正同学把两种无色液体混合时,也出现了同样的现象.| 假设 | |
| 固体物质 | |
| 无色液体 |
| 假设 | |
| 无色液体1 | |
| 无色液体2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com