
| A. | Cl2 NaCl | B. | N2O5 HNO3 | ||
| C. | MnO2 K2MnO4 | D. | P2O5 P2O3 |
分析 根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,结合各选项中的化学式进行解答本题.
解答 解:A、根据单质中元素的化合价为0,Cl2属于单质,故氯元素的化合价为0;钠元素显+1价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1价;带横线的同种元素的化合价不同,故选项错误.
B、五氧化二氮中氧元素显-2价,设氮元素的化合价是x,由在化合物中正负化合价代数和为零,可得:2x+(-2)×5=0,则x=+5价;氢元素显+1价,氧元素显-2价,设硝酸中氮元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+1)+y+(-2)×3=0,则y=+5价;带横线的同种元素的化合价相同,故选项正确.
C、氧元素显-2价,设二氧化锰中锰元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价;钾元素显+1价,氧元素显-2价,设锰酸钾中锰元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+1)×2+y+(-2)×4=0,则y=+6价;带横线的同种元素的化合价不同,故选项错误.
D、氧元素显-2价,设五氧化二磷中磷元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(-2)×5=0,则x=+5价;氧元素显-2价,设三氧化二磷中磷元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:2y+(-2)×3=0,则x=+3价;带横线的同种元素的化合价不相同,故选项错误.
故选:B.
点评 本题难度不大,掌握单质中元素的化合价为0、在化合物中正负化合价代数和为零并能灵活运用是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 利用光照和风力使水分蒸发得到食盐 | |
| B. | 利用海风使海水降温,从而使食盐结晶析出 | |
| C. | 利用光照使海水升温,从而使食盐析出 | |
| D. | 利用光照分解海水,从而制得食盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaCl、Ba(OH)2、HNO3 | B. | KOH、KNO3、CuCl2 | ||
| C. | NaOH、NaCl、Ba(OH)2 | D. | CuSO4、Ba(OH)2、BaCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g) | NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
| Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
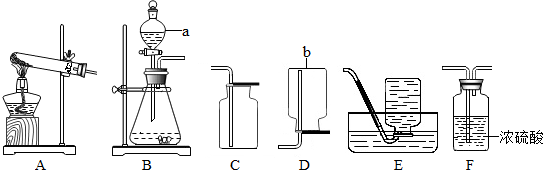
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
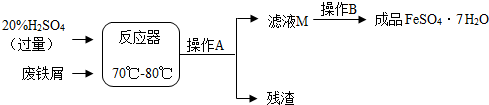
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NH3 | B. | HCl | C. | NO2 | D. | NO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com