
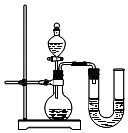
 如图是电解水的简易装置.回答下列问题:
如图是电解水的简易装置.回答下列问题:分析 (1)根据电解水实验的现象、结论分析回答;
(2)根据氧气的性质分析检验的方法;
(3)根据稀硫酸和氢氧化钠在溶于水时能解离出自由移动的离子分析回答;
(4)根据电解水实验的现象回答;
(5)根据水是由氢元素和氧元素组成的解答.
解答 解:(1)由电解水的装置可知,甲管生成的气体较多是氢气,乙管生成的气体较少是氧气,应接电源的正极,所以,b应接电源的正极;
(2)由于乙管中的气体是氧气能支持燃烧,所以,检验的方法是:将带火星的木条伸入试管内看是否复燃;
(3)由于稀硫酸和氢氧化钠在溶于水时能解离出自由移动的离子.所以,在实际操作时,常在水中滴加少量稀硫酸和氢氧化钠溶液,这是为了增强水的导电性;
(4)理论上甲、乙两试管中气体的体积比为2:1;
(5)水通电生成 氢气和氧气,说明水是由氢元素和氧元素组成的.
答案:
(1)氢气;正;
(2)用带火星的木条检验,木条复燃;
(3)增强水的导电性;
(4)2:1;
(5)氢元素和氧元素;
点评 熟练掌握电解水的实验,熟记其反应现象和结论,然后根据现象能够判断电池的正极和负极,记住六个字“正氧一,负氢二”.


科目:初中化学 来源: 题型:计算题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  两份等质量、等溶质质量分数的双氧水溶液在有无MnO2的情况下产生 | |
| B. |  向等质量的镁、锌中分别加入稀盐酸 | |
| C. |  向一定质量的稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液 | |
| D. |  室温下,向一定质量的饱和石灰水中加入氧化钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一个水分子是由两个氢气和一个氧气构成的 | |
| B. | 一个水分子是由两个氢元素和一个氧元素组成的 | |
| C. | 一个水分子是由两个氢原子和一个氧原子组成的 | |
| D. | 一个水分子是由两个氢原子和一个氧原子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 高锰酸钾 | 熟石灰 | 纯碱 |
| 化学式 | CH3COOH | KMnO4 | Ca(OH)2 | Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | X |
| 3 | 7.30% | 8.00% | 1 4 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某科学兴趣小组利用铜丝、铁丝、FeSO4溶液、CuSO4溶液、AgNO3溶液等实验药品,来探究铁、铜与银三种金属的化学活动性,并设计了如图所示的实验方案:将铁丝与铜丝分别浸入盛有CuSO4溶液和AgNO3溶液的两支试管中,观察实验现象.试回答下列问题:
某科学兴趣小组利用铜丝、铁丝、FeSO4溶液、CuSO4溶液、AgNO3溶液等实验药品,来探究铁、铜与银三种金属的化学活动性,并设计了如图所示的实验方案:将铁丝与铜丝分别浸入盛有CuSO4溶液和AgNO3溶液的两支试管中,观察实验现象.试回答下列问题: .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com