
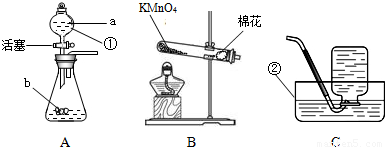
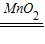 2H2O+O2↑; 后; 先用止水夹夹紧橡皮管(或关闭导管活塞),再往分液漏斗中注入一定量的水,打开分液漏斗活塞,一段时间后,漏斗内水不能进入锥形瓶,则装置气密性良好. (4)旋紧双孔胶塞 (5)拿掉;产生大量气泡和白雾;反应混合液通过导管进入水槽(其它合理答案也可). (6)发烫;放热反应 (7)①未除去铁丝表面的铁锈②收集的氧气纯度不够③未待火柴将近烧尽时伸入集气瓶中,瓶中氧气被火柴消耗. (8)带火星的木条复燃;集气瓶残留氧气浓度比空气含氧气浓度大
2H2O+O2↑; 后; 先用止水夹夹紧橡皮管(或关闭导管活塞),再往分液漏斗中注入一定量的水,打开分液漏斗活塞,一段时间后,漏斗内水不能进入锥形瓶,则装置气密性良好. (4)旋紧双孔胶塞 (5)拿掉;产生大量气泡和白雾;反应混合液通过导管进入水槽(其它合理答案也可). (6)发烫;放热反应 (7)①未除去铁丝表面的铁锈②收集的氧气纯度不够③未待火柴将近烧尽时伸入集气瓶中,瓶中氧气被火柴消耗. (8)带火星的木条复燃;集气瓶残留氧气浓度比空气含氧气浓度大

 全优点练单元计划系列答案
全优点练单元计划系列答案科目:初中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:初中化学 来源: 题型:
 过碳酸钠固体是过氧化氢和碳酸钠加合而成的化合物.其化学式为2Na2CO3?3H2O2,有关该化合物叙述如下.
过碳酸钠固体是过氧化氢和碳酸钠加合而成的化合物.其化学式为2Na2CO3?3H2O2,有关该化合物叙述如下.
| 实验序号 | 主要实验步骤及部分现象 |
| ① | 组装制取氧气的装置.选择的仪器(填序号) bdc或bdf bdc或bdf |
| ② | 检验装置的气密性(略). |
| ③ | 装药品的过程中,装入新配制的过碳酸钠溶液后,还需加入 二氧化锰 二氧化锰 (黑色固体).连接好装置,开始收集气体. |
| ④ | 在收集到气体中,伸入带火星的木条,木条复燃. |
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com