
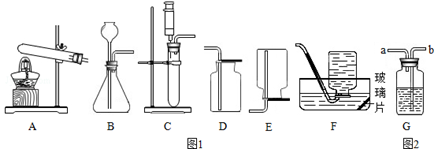
分析 (1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;注射器能够控制液体药品的流量,从而可以控制反应的速率;
氧气不易溶于水,所以收集较为纯净的氧气可用排水法;
(2)实验室通常用大理石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
洗气装置中导管长进短出;检验二氧化碳用澄清的石灰水;
(3)实验室常用氯化铵固体与碱石灰固体共热制取氨气,需要加热,属于固体加热型,常温下,氨气(NH3)是一种密度比空气小,易溶于水的气体,因此只能用向下排空气法收集.液氨泄漏时,可用喷水的方法除去空气中的氨气,说明氨气具有易溶于水的物理性质.根据发生液氨泄漏时正确的逃生方法是:用湿毛巾捂住口鼻、尽量贴近地面逃离解答.
解答 解:(1)实验室常用过氧化氢溶液和二氧化锰制取氧气,若要控制产生氧气的速率,应选择的发生装置是C,因为C装置中的注射器能够控制液体药品的流量,从而可以控制反应的速率;氧气不易溶于水,所以收集较为纯净的氧气可用排水法;该反应的化学方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)实验室常用大理石和稀盐酸制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
若用装置2干燥二氧化碳用浓硫酸,气体长进短出,与浓硫酸充分接触;检验二氧化碳用澄清的石灰水,二氧化碳与石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)实验室常用氯化铵固体与碱石灰固体共热制取氨气,需要加热,属于固体加热型,常温下,氨气(NH3)是一种密度比空气小,易溶于水的气体,因此只能用向下排空气法收集;液氨泄漏时,可用喷水的方法除去空气中的氨气,说明氨气具有溶于水的物理性质;发生液氨泄漏时正确的逃生方法是:用湿毛巾捂住口鼻;尽量贴近地面逃离.
故答案为:(1)C、F;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)CaCO3+2HCl=CaCl2+CO2↑+H2O;b;Ca(OH)2+CO2═CaCO3↓+H2O;
(3)A、E;溶于水;用湿毛巾捂住口(匍匐前进即可).
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.


科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | KCl(MnO2) | 加水溶解、过滤、洗涤、干燥 |
| B | CaO(CaCO3) | 加水溶解、过滤 |
| C | CO2(CO) | 通入适量氧气、点燃 |
| D | FeSO4溶液(H2SO4) | 加入过量Fe粉、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
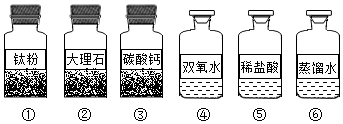
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ②③⑤ | C. | ①④ | D. | ②④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
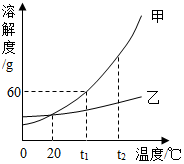
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | 除去CO2气体中的水蒸气 | 通过盛有浓硫酸的洗气瓶 |
| B | 分离CaO和CaCO3 | 加入足量蒸馏水,过滤烘干 |
| C | 除去NaCl溶液中的少量Ba(OH)2 | 加入过量稀硫酸 |
| D | 鉴别NH4Cl和NH4NO3 | 加入熟石灰研磨闻气味 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
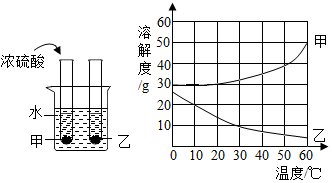
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com