
侯氏制“碱”法制得的纯碱中含有少量氯化钠。请根据下图所示的实验过程和提供的数据,回答下列问题: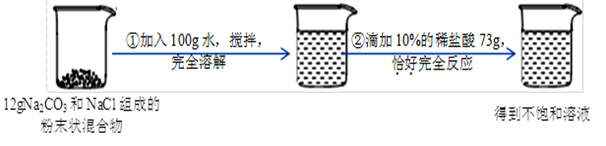
(1)在滴入稀盐酸的过程中,观察到的明显现象是 。
(2)该反应过程中生成CO2气体的质量.
(3)求最终所得溶液中溶质的质量是多少?
(1)固体逐渐溶解,产生气泡;
(2)4.4g;
(3)最终所得溶液中溶质的质量是13.1g
解析试题分析:分析反应可发现,混合物中加入稀盐酸恰好完全反应,由于生成了二氧化碳,所以可观察到实验的明显现象,利用反应的氯化氢的质量即可求出反应的碳酸钠质量和产生二氧化碳的质量和氯化钠的质量;利用碳酸钠的质量可求出生成的氯化钠的质量和原样品中氯化钠的质量,进而求出反应后溶质的质量:(1)由于碳酸钠和盐酸反应会生成二氧化碳,所以观察到的明显现象是固体逐渐溶解,产生气泡;
(2)设:样品中碳酸钠的质量为x,生成氯化钠的质量为y,生成二氧化碳的质量是z,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 117 44
x 73g×10% y z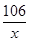 =
=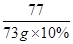 =
=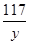 =
=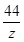
解得 x=10.6 g y=11.7 g z=4.4g
(3)∴样品中氯化钠的质量为13g-10.6g=1.4g;故反应后氯化钠的质量为:1.4g+11.7 g=13.1 g
考点:根据化学反应方程式的计算


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:初中化学 来源: 题型:计算题
(1)如图信息,瓶中溶液长期放置后溶质质量分数变小,是因为该物质具有 _性。(1分)
(2)某探究小组的同学对某工业废水(含有H2SO4、HNO3)中H2SO4的含量进行测定.取50g废水于烧杯中,加入足量BaCl2溶液、过滤、洗涤、干燥,得BaSO4固体11.65g.请解答下列问题:
①计算50g废水中H2SO4的溶质质量分数。(3分,要求写出计算过程)
②若改用KOH溶液(利用消耗的KOH的质量)测定50g废水中H2SO4
的含量,结果可能会 ____(选填“偏低”、“偏高”或“不变”),原因是_____________________________________。(每空1分,计2分)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(3分)现有一瓶久置的过氧化氢溶液(标签如图所示)。已知过氧化氢溶液在存放过程中会缓慢分解。取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g。
请计算:
(1)现该瓶溶液的溶质质量分数。
(2)用该瓶溶液配制100g溶质质量分数为3%的过氧化氢溶液需要加入水的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。他们为了测定水垢中碳酸钙的含量,将足量的盐酸加入到10g水垢中,产生CO2气体的情况如图所示。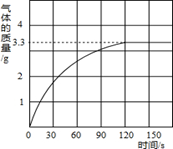
(1)从图中可以看出,10g水垢反应后生成的二氧化碳最多是 g。
(2)水垢中的碳酸钙质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
钛(Ti)是广泛应用于航空、航海等领域的一种重要金属。在一定条件下,钛由四氯化钛(TiCl4)和金属镁反应而制得:TiCl4+2Mg==Ti+2MgCl2 。现有380Kg四氯化钛,可生产金属钛多少千克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某烧杯中加入12.5 g含杂质的石灰石,与100 g稀盐酸恰好完全反应(杂质不与盐酸反应也不溶于水),称得烧杯中物质的总质量减少了4.4 g.求:
(1)石灰石含碳酸钙的质量分数.
(2)反应后溶液中溶质的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
鸡蛋壳的主要成分是碳酸钙,为了测定鸡蛋壳中碳酸钙的含量,小丽称取30g干燥的碎鸡蛋壳放入烧杯中,并向其中加入了80g稀盐酸恰好完全反应(假设鸡蛋壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应),反应后烧杯中物质的总质量为101.2g。我能完成下列计算:
⑴碳酸钙的质量;
⑵当碳酸钙恰好完全反应时所得溶液中溶质的质量分数。(结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
宇航员在太空舱中,往往可利用自己呼出的二氧化碳与过氧化钠粉末作用来获得所需的氧气,并合理处理呼出的二氧化碳。(反应方程式为2Na2O2+2CO2===2Na2CO3+O2)假如某宇航员在某次太空飞行中预计消耗氧气480kg,则该宇航员应在太空舱中至少准备多少kg过氧化钠。(要求写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
用“侯氏制碱法”制得的纯碱常含有少量的氯化钠(假定只含氯化钠杂质):某化学兴趣小组为了测量纯碱样品中碳酸钠的质量分数,做了如下实验:称量某纯碱样品12 g,加入到足量的氯化钡溶液中,恰好完全反应。过滤干燥后,称得沉淀质量为19.7g。
请计算:纯碱样品中碳酸钠的质量分数(计算结果精确到0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com