
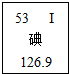
 碘元素是人体必须的微量元素之一
碘元素是人体必须的微量元素之一分析 (1)根据元素周期表中的一个小格所提供的信息,其中原子序数=核外电子数=质子数=核电荷数,进行解答;
(2)①氯化钠是由钠元素和氯元素组成的化合物,化学式为NaCl;氯化钠含有的阴离子是Cl-;
②根据质量守恒定律反应中前后原子个数不变解答.
解答 解:(1)根据元素周期表中的一个小格所提供的信息,可知碘原子的核电荷数是 53,
(2)①氯化钠是由钠元素和氯元素组成的化合物,化学式为NaCl;氯化钠含有的阴离子是氯离子;表示为:Cl-;
②根据反应的化学方程式KIO3+5X+3H2SO4=3K2SO4+3I2+3H2O,反应后K、S、O、I、H元素的原子个数分别为6、3、15、6、6,而反应前除5个X分子外K、S、O、I、H元素的原子个数分别为1、3、15、1、6;根据反应前后原子个数不变,可判断5个X分子中应含有5个钾原子和5个碘原子,则每个X分子由1个钾原子、1个碘原子所构成,所以,物质X的化学式为KI
答案:(1)53 非金属
(2)①Cl-;②KI.
点评 本题考查学生对化合价计算能力;考查学生运用质量守恒定律推断化学式的能力.此类问题是有关质量守恒定律的常见题,根据化学方程式,得出未知的化学式中所含元素的原子个数,即可推断出化学式.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:初中化学 来源: 题型:多选题
| A. | 铁钉放入硫酸铜溶液中,溶液由蓝色变为浅绿色 | |
| B. | 硫酸铜溶液和氢氧化钠溶液反应生成蓝色沉淀 | |
| C. | 红磷在空气中燃烧产生,产生大量白色烟雾 | |
| D. | 将空气中燃着的硫伸入氧气瓶中,火焰由黄色变为蓝紫色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生活中改变不良的用水习惯,尽可能充分利用每一滴水 | |
| B. | 农业生活中改变灌溉方式,变漫灌为喷灌或滴灌,以节约用水 | |
| C. | 城市生活污水、工业废水应遵循“先净化,后排放”的原则 | |
| D. | 往江河里倾倒垃圾 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
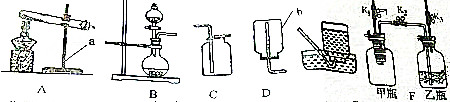 如图是实验室常用的实验装置,请根据要求填空:
如图是实验室常用的实验装置,请根据要求填空:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | 实验操作 | 实验现象 |
| ① | 在试管中加入过氧化氢溶液,然后将带火星的木条伸入试管中 | 产生少量气泡,木条不复燃 |
| ② | 在装有过氧化氢溶液的试管中加入1g四氧化三铁,然后将带火星的木条伸入试管中 | 产生大量气泡,木条 复燃 |
| ③ | 待②中反应结束,将试管中的剩余物进行过滤、洗涤、干燥、称量 | 称得固体质量为1g |
| ④ | 将③中所得固体放入试管中,滴入足量的稀硫酸,充分震荡 | 产生大量气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁锈放入稀盐酸中溶液变绿色 | |
| B. | 酚酞试液滴入硫酸溶液中变红色 | |
| C. | 硫在氧气中燃烧发出微弱的淡蓝色火焰 | |
| D. | 硫酸铜溶液中滴加氢氧化钠溶液出现蓝色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com