
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 操作方法 |
| A | CaO粉末(CaCO3粉末) | 加足量的水,充分搅拌后过滤 |
| B | Fe(Fe2O3) | 加入过量稀盐酸,充分反应后过滤 |
| C | CuSO4溶液(H2SO4) | 加入过量氧化铜粉末,加热,充分反应后过滤 |
| D | CO2(HCl) | 通过盛有氢氧化钠溶液的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 细铁丝在氧气中燃烧,火星四射,生成黑色固体 | |
| B. | 红磷在空气中燃烧产生大量的白色烟雾 | |
| C. | 硫在氧气中燃烧产生蓝紫色火焰、放热、生成有刺激性气味的气体 | |
| D. | 打开盛有浓盐酸试剂瓶的瓶塞,在瓶口上方出现大量白雾 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | 盐酸的质量分数/% | 反应温度/℃ | 铁锈消失的时间/s |
| ① | 6 | 20 | 240 |
| ② | 10 | 20 | 115 |
| 实验编号 | 硫酸的质量分数/% | 反应温度/℃ | 铁锈消失的时间/s |
| ③ | 6 | 20 | 310 |
| ④ | 10 | 20 | 155 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
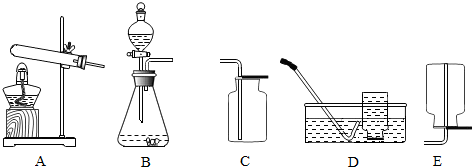
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加热碳酸氢铵,白色固体逐渐消失,并产生刺激性气味 | |
| B. | 加热碱式碳酸铜,黑色固体变成绿色固体 | |
| C. | 木炭在氧气中燃烧,发出白光并放出大量的热 | |
| D. | 细铁丝在氧气中燃烧,火星四射,生成黑色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | X | O2 | CO2 | H2O |
| 反应前质量/g | 16 | 70 | 1 | 0 |
| 反应后质量/g | 0 | 待测 | 45 | 36 |
| A. | 该反应为置换反应 | |
| B. | X中一定只含有碳、氢两种元素 | |
| C. | 表中“待测”值为5 | |
| D. | 反应生成的CO2和H2O的质量比为45:36 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com