
| A. | CO2中有少量HCl气体(氢氧化钠溶液) | B. | NH4Cl中有杂质KCl(氢氧化钾) | ||
| C. | FeSO4溶液中有杂质CuSO4(铁粉) | D. | NaCl中有杂质MgCl2(氢氧化钙) |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所用的药品错误.
B、NH4Cl能与氢氧化钾反应生成氯化钾、氨气和水,反而会把原物质除去,不符合除杂原则,故选项所用的药品错误.
C、铁粉能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所用的药品正确.
D、MgCl2能与氢氧化钙溶液反应生成氢氧化镁沉淀和氯化钙,能除去杂质但引入了新的杂质氯化钙,不符合除杂原则,故选项所用的药品错误.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:初中化学 来源: 题型:选择题
| 选项 | 物质(杂质) | 操作方法 |
| A | CO2(CO) | 将气体点燃 |
| B | CaO(CaCO3) | 加足量稀盐酸、过滤 |
| C | KNO3(NaCl) | 蒸发结晶、过滤 |
| D | FeCl2(CuCl2) | 加入足量铁屑,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
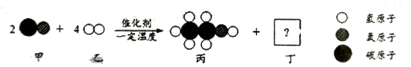
| A. | 甲中碳元素的化合价为+2价 | B. | 丙中C、H、O的质量比为12:3:8 | ||
| C. | 丁的化学式为H2O2 | D. | 该反应体现无机物可转化为有机物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO32-、SO42-、Mg2+ | B. | Cl-、K+、Cu2+ | ||
| C. | Cl-、NO3-、Na+ | D. | SO42+、Ba2+、K+ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 0.8g | B. | 1.0g | C. | 1.2g | D. | 1.4g |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
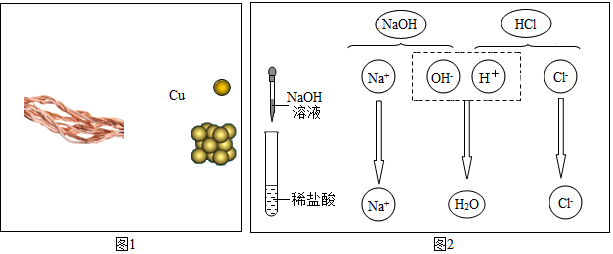

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
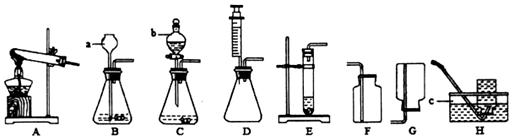
| 可能的原因 | 实验步骤 | 实验现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com