
| 实验步骤 | 实验现象 | 实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水 充分混合后静置,取少量上层清液,滴加1~2滴无色酚酞试液 | 溶液变成红色 | 该样品还含有氢氧化钙 |
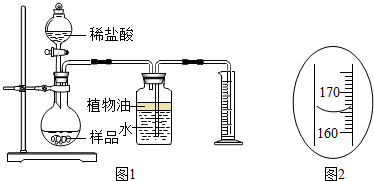
分析 (1)根据氢氧化钙和二氧化碳反应产生碳酸钙沉淀和水写出反应的方程式;
(2)根据氢氧化钙溶液显碱性设计实验并描述现象;
(3)根据碳酸钙和盐酸反应产生氯化钙、水和二氧化碳,写出反应的方程式并描述现象;
(4)根据实验目的分析量筒的作用;
(5)根据量筒的读数方法读数并进行化学方程式的计算;
(6)根据实验目的分析可能产生的误差原因.
解答 解:(1)氢氧化钙和二氧化碳反应产生碳酸钙沉淀和水,故反应的方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;故答案为:CO2+Ca(OH)2═CaCO3↓+H2O;
(2)氢氧化钙溶液显碱性,能够使酚酞试液变成红色,因此可以取少量上层清液,滴加1~2滴无色酚酞试液(或其他合理答案);溶液变成红色(或其他合理答案);故答案为:取少量上层清液,滴加1~2滴无色酚酞试液(或其他合理答案);溶液变成红色(或其他合理答案);
(3)滴加稀盐酸和碳酸钙反应产生二氧化碳,至不再产生气泡时说明碳酸钙反应完全,碳酸钙和盐酸反应产生氯化钙、水和二氧化碳;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;无气泡产生;
(4)要测定反应产生二氧化碳的体积,通过气压的增大把水压入量筒,量筒内水的体积就是二氧化碳的体积;故答案为:根据进入量筒内水的体积,测量生成的CO2的体积(或其他合理答案);
(5)读数时视线与凹液面的最低处保持水平,因此读数为165mL,即0.165L,二氧化碳的密度为2g•L-1,因此二氧化碳的质量为0.33g.
设碳酸钙的质量分数为x,则样品中碳酸钙的质量为3xg,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
3xg 3.3g
$\frac{100}{3xg}=\frac{44}{3.3g}$ x=25%
故答案为:165;25%;
(6)在实验过程中无法考虑盐酸加入后烧瓶内物质所占体积的变化对测定数据产生的影响,可能会对测定样品中R的质量分数产生一定的影响;
故答案为:无法考虑盐酸加入后烧瓶内物质所占体积的变化对测定数据产生的影响(或稀盐酸具有挥发性,产生的气体中可能混有氯化氢气体,或其他合理答案).
点评 本题从定性和定量的两个角度探究了氢氧化钙的变质程度及变质程度的计算,难度较大,解题的关键是明确氢氧化钙、碳酸钙等的性质及测定的原理.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 8g | B. | 16g | C. | 32g | D. | 4g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
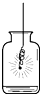 火锅,古称“古董羹”,因食物投入沸水时发出的“咕咚”声而得名,它是中国独创的美食,历史悠久.
火锅,古称“古董羹”,因食物投入沸水时发出的“咕咚”声而得名,它是中国独创的美食,历史悠久.| 实验步骤 | (1)预先在集气瓶中放入少量水,其作用是防止铁燃烧形成的高温熔融物溅落时炸裂集气瓶. (2)待火柴快燃尽时,再将铁丝伸入盛有氧气的集气瓶中. “火柴快要燃尽时再伸入集气瓶中”的目的是充分加热铁,同时减少火柴消耗氧气. |
| 实验现象 | 铁丝剧烈燃烧,火星四射,放出大量热,生成一种黑色固体. |
| 实验结论 | 该反应的化学方程式是3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
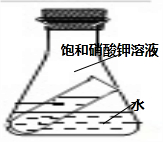 明明同学设计了如图所示的装置进行趣味实验.
明明同学设计了如图所示的装置进行趣味实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com