

| 硝酸银溶液的质量 | 铜粉的质量 | 铁粉的质量 | 所得滤渣的质量 | |
| 实验1 | 200g | 3.2g | 2.8g | 21.6g |
| 实验2 | 200g | 4.8g | 2.8g | 23.2g |
| 实验3 | 200g | 3.2g | 5.6g | 24.8g |
| 实验4 | 200g | 4.8g | 5.6g | 26.4g |
分析 (1)根据铁和硝酸银反应生成硝酸亚铁和银,铜和硝酸银反应生成硝酸铜和银进行分析;
(2)根据铁、铜、银的活动性顺序为:铁>铜>银,所以将铁粉和铜粉的混合物加入硝酸银中,铜会先于硝酸银反应,然后铁再与硝酸银反应进行分析;
(3)根据参加反应的铁的质量和化学方程式进行计算;
(4)根据化学方程式计算硝酸银溶液中的溶质质量,然后计算加入水的质量;
(5)根据溶液稀释前后,溶质质量分数不变进行分析.
解答 解:(1)铁和硝酸银反应生成硝酸亚铁和银,铜和硝酸银反应生成硝酸铜和银,化学方程式为:Fe+2AgNO3═Fe(NO3)2+2Ag,Cu+2AgNO3═Cu(NO3)2+2Ag;
(2)铁、铜、银的活动性顺序为:铁>铜>银,所以将铁粉和铜粉的混合物加入硝酸银中,铜会先于硝酸银反应,然后铁再与硝酸银反应,铜的质量增大1.6g,滤渣的质量也增大1.6g,所以实验2后滤渣的成分为:铜、银;
(3)设置换出的银的质量为x
Fe+2AgNO3═Fe(NO3)2+2Ag
56 216
2.8g x
$\frac{56}{2.8g}$=$\frac{216}{x}$
(3)通过对比实验1、3可知,铁的质量增大一倍,实验1中置换出银:21.6g,实验3中置换出银:24.8g,所以实验3中的硝酸银完全反应,所以
设与铁反应的硝酸银的质量为y,生成硝酸亚铁为m,与铜反应的硝酸银的质量为z,生成硝酸铜质量为n
Fe+2AgNO3═Fe(NO3)2+2Ag
56 340 180
5.6g y m
$\frac{56}{5.6g}$=$\frac{340}{y}$=$\frac{180}{m}$
y=34g
m=18g
Cu+2AgNO3═Cu(NO3)2+2Ag;
64 340 188
3.2g z n
$\frac{64}{3.2g}$=$\frac{340}{z}$=$\frac{188}{n}$
z=17g
n=18.8g
所以用硝酸银固体配制实验中所需的硝酸银溶液,需要水的质量为200g-17g-34g=149g;
(4)向实验3所得滤液中加入16g水,此时溶液中溶质的质量分数为:$\frac{18g+18.8g}{200g+3.2g+5.6g-24.8g+16g}$×100%=18.4%.
故答案为:(1)Fe+2AgNO3═Fe(NO3)2+2Ag,Cu+2AgNO3═Cu(NO3)2+2Ag;
(2)铜、银;
(3)$\frac{56}{2.8g}$=$\frac{216}{x}$
(3)149g;
(4)18.4%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
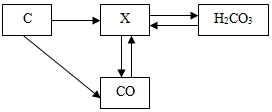 在C、H、O、Na、Cl、Ca六种元素中选择合适的按要求填空:
在C、H、O、Na、Cl、Ca六种元素中选择合适的按要求填空:查看答案和解析>>
科目:初中化学 来源: 题型:推断题
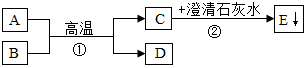
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 预期现象与结论 |
| 步骤1:取少量固体样品于 试管中,加入足量的蒸馏水, 充分振荡. | 若得到澄清溶液,说明样品中含有碳酸钠和硫酸钠; 若产生白色沉淀,则继续进行实验. |
步骤2:往步骤1的试管中继续加入足量的稀HNO3 | 若沉淀完全溶解,说明样品中含有硝酸钡和碳酸钠; 若沉淀完全不溶解,说明样品中含有硝酸钡和硫酸钠; 若沉淀部分溶解且有气泡产生,说明样品中含有碳酸钠、硫酸钠和硝酸钡 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

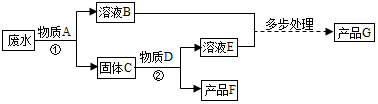
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com