
| 序号 | 实验步骤 | 简述实验操作(不必叙述如何组装实验装置) |
| ① | 溶解 | 将混合物放入烧杯中,加水,充分搅拌直到固体不再溶解. |
| ② | ||
| ③ | ||
| ④ | ||
| ⑤ | 过滤、干燥 | 得到K2Cr2O7晶体 |

| 各个生成物平衡浓度的系数次方的乘积 |
| 各个反应物平衡浓度系数次方的乘积 |
| c(CO2)8 |
| c(O2)7 |
| c(CO2)8 |
| c(O2)7 |
| ||
| ||
| c(CO2)8 |
| c(O2)7 |
| ② | 蒸发 | 将所得溶液转移至蒸发皿中,加热蒸发溶液,使NaC1结晶析出 |
| ③ | 过滤 | 趁热过滤,将NaC1晶体与溶液分离 |
| ④ | 冷却,结晶 | 冷却滤液使K2Cr2O7结晶析出 |


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案科目:初中化学 来源: 题型:
| A、纯净物一定由同种元素组成 |
| B、化合物一定由不同种元素组成 |
| C、氧化物一定由两种元素组成 |
| D、混合物一定由多种物质混合而成 |
查看答案和解析>>
科目:初中化学 来源: 题型:
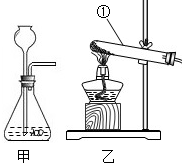 如图是实验室制取氧气的两种发生装置.请回答下列问题:
如图是实验室制取氧气的两种发生装置.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
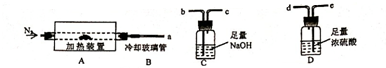
| A、样品的质量 |
| B、装置C的增重 |
| C、样品的质量和装置C的增重 |
| D、样品分解后残余物质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:
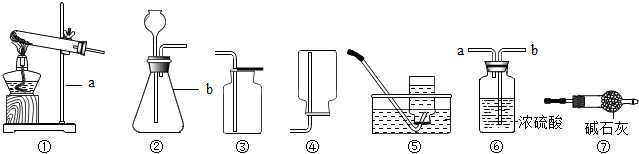
查看答案和解析>>
科目:初中化学 来源: 题型:
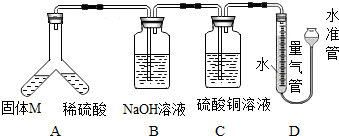
查看答案和解析>>
科目:初中化学 来源: 题型:
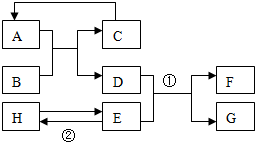 已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答:
已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
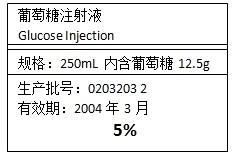 如图是病人输液时用的一瓶葡萄糖注射液标签,请你据图回答下列问题:
如图是病人输液时用的一瓶葡萄糖注射液标签,请你据图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com