
 桐桐采集了一块石灰石样品,该样品杂质只含二氧化硅(二氧化硅是一种既不溶于水也不与盐酸反应且耐高温的固体).
桐桐采集了一块石灰石样品,该样品杂质只含二氧化硅(二氧化硅是一种既不溶于水也不与盐酸反应且耐高温的固体).分析 (1)在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.
(2)根据质量守恒定律分析样品质量,根据反应时间曲线可查出碳酸钙完全反应后放出气体二氧化碳的质量,利用生成二氧化碳的质量计算出所取样品中碳酸钙质量,碳酸钙质量与样品质量比即样品中碳酸的质量分数.
解答 解:(1)在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,故选B装置.故填B;
(2)样品质量为76g-20g-50g=6g;故答案为:6;
①为避免样品中碳酸钙不能完成反应,可把样品粉碎,增大样品与盐酸的接触面积,此举还可以加快反应的速率;
故答案为:增大石灰石与盐酸的接触面积使碳酸钙更充分反应;加快反应速率.
②图中质量轴上每个小刻度表示0.2g,所以完全放出气体后剩余物质总质量为73.8g;
根据质量守恒定律,因此放出气体二氧化碳的质量=76g-73.8g=2.2g
故答案为:2.2g;
③设石灰石样品中碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 2.2g
$\frac{100}{x}$=$\frac{44}{2.2g}$
解之得 x=5g
石灰石样品中碳酸钙的质量分数=$\frac{5g}{6g}$×100%=83.3%.
答:该石灰石样品中碳酸钙的质量分数是83.3%.
点评 准确判断图中刻度值是正确解决本题一个重要细节,是正确判断生成二氧化碳质量的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
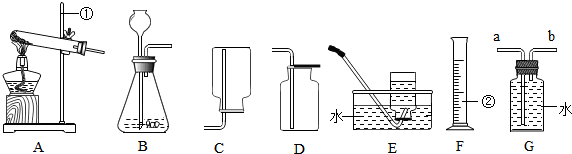
| A. | ① | B. | ② | C. | ③ | D. | 全都可以 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
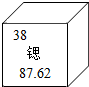 美国物理学家研制出迄今最精确的“锶晶格原子钟”,运行50亿年也不会偏差1秒.根据如图,下列说法正确的是( )
美国物理学家研制出迄今最精确的“锶晶格原子钟”,运行50亿年也不会偏差1秒.根据如图,下列说法正确的是( )| A. | 锶原子的中子数是38 | |
| B. | 锶的元素符号为SR | |
| C. | 锶元素原子的相对原子质量为87.62g | |
| D. | 锶这种物质由原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
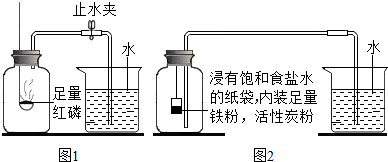
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
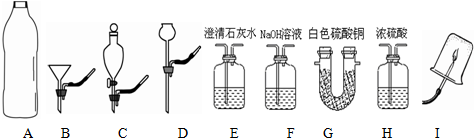
| 实验序号 | 实验1 | 实验2 | 实验3 |
| 实验操作 |  |  | 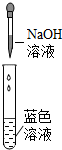 |
| 实验现象 | 铁丝表面出现红色物质 | 产生白色沉淀,甲稀NHO3后沉淀不溶解 | 产生蓝色絮状沉淀 |
| 实验结论 | 可能含有Cu元素 | (1)白色沉淀是硫酸钡 | (2)“蓝色水”中含有溶质的化学式是CuSO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com