
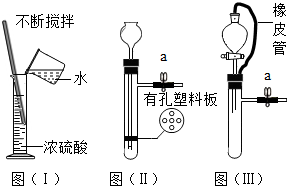
分析 (1)稀释浓硫酸时,一定要把浓硫酸沿着容器壁慢慢注入水中,同时用玻璃棒不断的搅拌,使产生的热量迅速散失,且配制溶液通常用烧杯,量筒不能用来配制溶液.
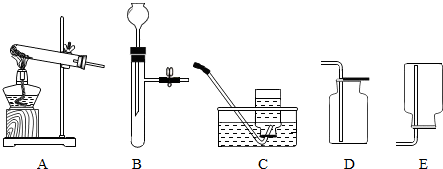
(2)据反应物状态和反应条件选择发生装置,据气体密度和溶解性选择收集装置;
(3)据检查装置气密性的方法分析解答;
(4)据实验室常用大理石和稀盐酸反应制取二氧化碳,装置特点分析解答;
(5)分液漏斗与长颈漏斗相比,可以通过控制滴加液体的速度或流速、流量等来控制反应的速度.
解答 解:(1)稀释浓硫酸时,一定要把浓硫酸沿着容器壁慢慢注入水中,同时用玻璃棒不断的搅拌,使产生的热量迅速散失,且配制溶液通常用烧杯,量筒不能用来配制溶液,只能用来量取液体的体积;
(2)实验室制取氢气用锌粒和稀硫酸常温反应,故选发生装置B,氢气密度比空气小且难溶于水,所以可用向下排空气法或排水法收集;
(3)检查该装置气密性的方法:A打开止水夹a,手握住试管一会儿发现伸入水槽的导管口无汽泡冒出说明装置的气密性不好;C打开止水夹a,往长颈漏斗里注水,使长颈漏斗下管口在水面的上方,手握住液面以上的试管,发现伸入水槽的导管口无汽泡冒出,说明装置的气密性不好;这两个选项都有两个出气口,气体受热膨胀也会从长颈漏斗逸出,故不可行;正确方法是B:先关闭止水夹a,往长颈漏斗里注水,当长颈漏斗内水面高于试管内水面时,停止加水,观察一段时间,发现长颈漏斗内、外水面高度差不变,说明装置的气密性好;
(4)实验室制取二氧化碳常用大理石和稀盐酸反应;关闭止水夹后,产生的气体不能出来,产生的压力使液体被压倒长颈漏斗中,固液分离,反应停止;
(5)与B装置相比较,图(Ⅲ)装置以分液漏斗代替长颈漏斗,可逐滴滴加液体,从而能够控制反应速率;
故答案为:
(1)将水倒入浓硫酸中;用量筒作为配制容器;
(2)BC(或BE);
(3)B;
(4)②③;液体被压回长颈漏斗中,固液分离,反应停止;
(5)能够控制反应速率.
点评 本题主要考查了学生对实验室制取气体的相关知识的掌握和运用知识分析、解决问题的能力,能较好培养学生的能力.合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:实验探究题
 一天,实验助手小林走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
一天,实验助手小林走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 它们是两种新型的化合物 | B. | 它们是由碳元素形成的两种单质 | ||
| C. | 它们的化学性质是完全相同的 | D. | 它们的相对分子质量相差为120 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 水蒸气能点燃火柴吗?做如图所示实验,加热烧瓶中的水使之沸腾,水蒸气通过加热的铜管喷出;把火柴靠近铜管口处,火柴被加热;迅速从蒸汽中移开,火柴燃着了.
水蒸气能点燃火柴吗?做如图所示实验,加热烧瓶中的水使之沸腾,水蒸气通过加热的铜管喷出;把火柴靠近铜管口处,火柴被加热;迅速从蒸汽中移开,火柴燃着了.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
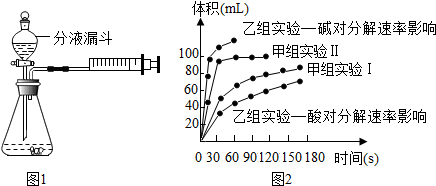
| 实验编号 | 温度 | 催化剂 | 质量分数 | |
| 甲组实验Ⅰ | 25℃ | 二氧化锰 | 10mL 2%H2O2 | |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com