
| 离子 | OH- | Cl- | SO42- |
| H+ | 溶、挥 | 溶 | |
| Na+ | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 微 |
| Cu2+ | 不 | 溶 | 溶 |
 考前必练系列答案
考前必练系列答案科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 洗涤后排出的液体一定是溶液 | |
| B. | 洗涤后衣服上一定没有残留洗涤剂 | |
| C. | 洗涤剂加水稀释后,溶质质量分数变大 | |
| D. | 洗涤时适当提高水温,能加快洗衣粉溶解 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用食用白醋洗涤 | B. | 用食盐水洗涤 | C. | 用洗洁精洗涤 | D. | 用肥皂水洗涤 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
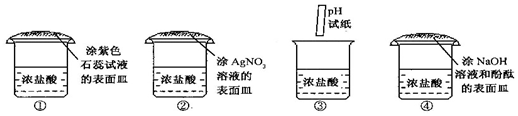
| A. | ①② | B. | ②④ | C. | ①③④ | D. | ①③ |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 中子数为117的原子,相对原子质量为117 | |
| B. | 中子数为118的原子,核外有118个电子 | |
| C. | 这两种原子互为同位素原子 | |
| D. | 因为两种原子的质子数相同,所以两种原子的质量也相同 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
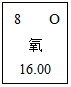 如图是元素周期表中氧元素的信息示意图,下列有关氧的说法错误的是( )
如图是元素周期表中氧元素的信息示意图,下列有关氧的说法错误的是( )| A. | 氧是地壳中含量最高的非金属元素 | |
| B. | 氧原子的相对原子质量为16.00 | |
| C. | 氧原子的质子数为8 | |
| D. | 氧气在空气中所占的质量比约为21% |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com