
| 氢氧化钠溶液 | 氯化钠溶液 | 碳酸钠溶液 | 氯化钡溶液 | |
| 稀硫酸 | A组 | B组 | C组 | D组 |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
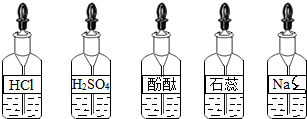
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中 | 猜想②正确 相关的化学方程式 |
查看答案和解析>>
科目:初中化学 来源: 题型:
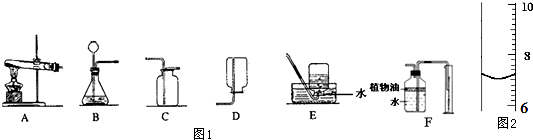
查看答案和解析>>
科目:初中化学 来源: 题型:
 称取一定量的BaCl2的固体加水配成100g溶液,然后向该溶液中逐滴加入Na2SO4溶液,到反应终点(恰好完全反应)时消耗的Na2SO4溶液质量为100克,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4↓+2NaCl)
称取一定量的BaCl2的固体加水配成100g溶液,然后向该溶液中逐滴加入Na2SO4溶液,到反应终点(恰好完全反应)时消耗的Na2SO4溶液质量为100克,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4↓+2NaCl)查看答案和解析>>
科目:初中化学 来源: 题型:
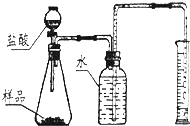 某兴趣小组把一块固体氢氧化钠放在表面皿里,长时间暴露在空气中,发现固体表面逐渐湿润,部分溶化成液体后又逐渐形成晶体,最终变成粉末.请回答下列问题:
某兴趣小组把一块固体氢氧化钠放在表面皿里,长时间暴露在空气中,发现固体表面逐渐湿润,部分溶化成液体后又逐渐形成晶体,最终变成粉末.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com