
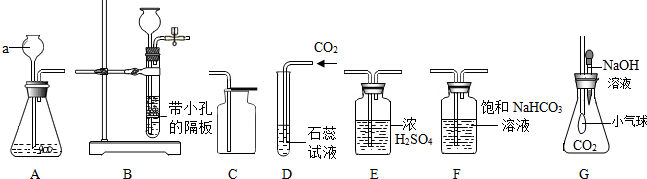
| A. | 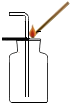 检验CO2是否收集满 | B. | 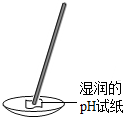 测试某溶液的酸碱度 | ||
| C. | 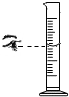 量取3mL液体 | D. | 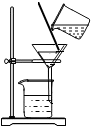 分离溶液中的固态物质 |
分析 A、根据二氧化碳的验满方法进行分析判断.
B、根据溶液酸碱度的测定方法,进行分析解答.
C、根据量筒的使用方法方法判断.
D、分离溶液中的固态物质可用过滤.
解答 解:A、检验CO2是否收集满,应将燃着的木条放在集气瓶口,不能伸入瓶中,图中所示操作正确.
B、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH,如用润湿的pH试纸测酸性pH偏大,测碱性pH偏小,图中所示操作错误.
C、用量筒量取液体时,视线与凹液面的最低处保持平衡,图中所示操作正确.
D、过滤可以分离出液体中的固体,图中所示操作正确.
故选B.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
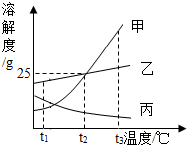 如图是甲、乙、丙三种固体物质溶解度曲线,下列叙述正确的( )
如图是甲、乙、丙三种固体物质溶解度曲线,下列叙述正确的( )| A. | t2℃时乙物质的饱和溶液溶质的质量分数为20% | |
| B. | t2℃时三种物质溶解度关系为:甲>乙>丙 | |
| C. | 随温度的升高,甲、乙、丙三种物质溶解度都增大 | |
| D. | 甲物质的饱和溶液从t1℃升温到t3℃时,溶质质量分数增大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
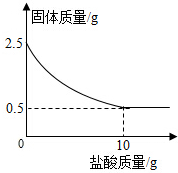 测定石灰石中的碳酸钙的含量,取出2.5克石灰石样品,逐渐加入稀盐酸,充分反应后测得剩余固体质量与加入稀盐酸的质量关系如图所示.
测定石灰石中的碳酸钙的含量,取出2.5克石灰石样品,逐渐加入稀盐酸,充分反应后测得剩余固体质量与加入稀盐酸的质量关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
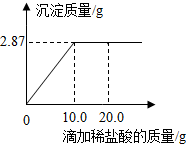 为测定某AgNO3溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定.现取待测液50.0g,滴定过程如图所示.
为测定某AgNO3溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定.现取待测液50.0g,滴定过程如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 试剂 | 操作方法 | 反应类型 |
| A | MnO2 | KCl | 适量水 | 溶解、过滤、蒸发结晶 | / |
| B | CO2 | CO | 足量氧气 | 点燃 | 化合反应 |
| C | CaO | CaCO3 | 稀盐酸 | 过滤 | 复分解反应 |
| D | NaOH溶液 | Ca(OH)2 | 适量Na2CO3溶液 | 过滤 | 复分解反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 低钠盐是一种健康食盐,以普通钠盐为基础添加一定量氯化钠(氯化钠70%左右,氯化钾30%左右),有助于人体钠、钾平衡,降低高血压、心血管疾病的患病风险.另外,由于食盐中导致咸味的是氯离子,因此,低钠盐能较好实现减钠补钾不减咸味的目的.
低钠盐是一种健康食盐,以普通钠盐为基础添加一定量氯化钠(氯化钠70%左右,氯化钾30%左右),有助于人体钠、钾平衡,降低高血压、心血管疾病的患病风险.另外,由于食盐中导致咸味的是氯离子,因此,低钠盐能较好实现减钠补钾不减咸味的目的.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com