
(10分)通过实验对草酸(相对分子质量是90)进行如下研究。
【查阅资料】①浓硫酸常作干燥剂 ②浓NaOH溶液常用于吸收CO2气体
③无水硫酸铜吸水后由白色变为蓝色 ④氯化钯(PdCl2)溶液遇CO产生黑色沉淀
【实验准备】选用下列实验装置(气密性良好,部分固定装置已略去):
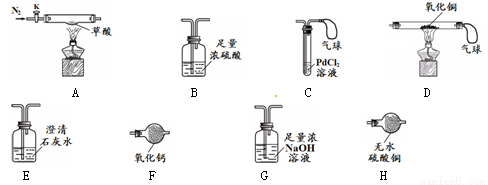
【实验I】检验草酸分解的产物。
实验步骤 | 实验现象 | 实验结论及分析 |
(1)按A→H→E→C 连接仪器 (2)关闭K,点燃A处酒精灯 | H中 E中澄清石灰水变浑浊 C中产生黑色沉淀,气球鼓起 | 草酸分解生成了CO2、CO和H2O ①E中反应的化学方程式是 ②C中气球的作用是 |
【实验II】取9 g草酸进行实验,测定生成物的质量并确定草酸的组成。
实验步骤 | 实验数据 | 实验结论及分析 |
(1)选择A、B、D、G装置组合进行实验 (2)鼓入过量的N2后,分别称量B、D、G的质量 (3)关闭K,点燃A、D处的酒精灯,至草酸完全分解 (4)熄灭A处酒精灯,通入过量的N2,熄灭D处酒精灯,再次分别称量B、D、G的质量 | B装置增重1.8 g D装置中固体 质量减少0.8 g G装置增重4.4 g | ①A、B、D、G装置的正确连接顺序是A→ → →D ②向A中两次通入N2,其中 第二次的目的是 ③草酸的化学式是 ④反思:若用F代替B,则不能测定草酸的组成,其原因是 |
【实验I】 白色固体变成蓝色
①Ca(OH)2 + CO2  CaCO3↓+ H2O
CaCO3↓+ H2O
②收集尾气(或尾气处理装置)
【实验II】①B→G
②将生成的气体完全排入吸收装置,使其被完全吸收
③C2H2O4
④CaO可同时吸收H2O、CO2,导致无法准确测量H2O、CO2的质量
【解析】
试题分析:【实验I】根据资料:若草酸分解的产物中含有水,那么H中的无水硫酸铜会变成蓝色;若生成了二氧化碳,那么E中的澄清石灰水会变浑浊;若产生了一氧化碳,那么C中的氯化钯(PdCl2)溶液会变成黑色;由于一氧化碳有毒,直接排放到空气中会污染空气,故要要尾气处理装置,气球可用于收集尾气;
【实验II】①由于草酸分解生成了水、二氧化碳和一氧化碳。由于气体溶液中含有水,故要先把水吸收以免造成实验结果偏大,而水直接利用浓硫酸吸收即可;检验一氧化碳是利用一氧化碳的的还原性呈二氧化碳来判断,那么要先利用氢氧化钠溶液将二氧化碳吸收掉,然后再把气体通入氧化铜中,故顺序是A→B→G→D;
②向A中两次通入N2,其中第二次的目的是将生成的气体完全排入吸收装置,使其被完全吸收;
③B装置增重1.8 g,说明分解生成的水的质量为1.8g,那么氢元素的质量=1.8g×2/18 =0.2g,氧元素的质量为1.6g;G装置增重4.4 g,说明生成的二氧化碳的质量为4.4g,那么碳元素的质量为4.4g×12/44 =1.2g,氧元素的质量为3.2g,;D装置中固体质量减少0.8 g,说明氧化铜中氧元素的质量为0.8g,那么氧化铜是质量=0.8g /(16/80)=4g,利用化学方程式即可计算出一氧化碳的质量1.4g,那么碳元素的质量为1.4g×12/28 =0.6g,那么氧元素的质量为0.8g。综合上述计算,草酸中碳元素的质量=1.2g+0.6g=1.8g,氧元素的质量=1.6g+3.2g+0.8g=5.6g;氢元素的质量=0.2g。依据质量守恒定律化学反应前后物质的总质量不变可知草酸的质量为1.8g+4.4g+1.4g=7.6g,设氢原子的个数为x,那么7.6g× x/90 =0.2g,x=2,设碳原子的个数为y,那么7.6g× 12y/90 =1.8g,y=2,氧原子的个数为z,那么7.6g× z/90 =5.6g,z=4,故草酸的化学式为C2H2O4;
④由于CaO可同时吸收H2O、CO2,导致无法准确测量H2O、CO2的质量,故不能测定出草酸的组成。
考点:物质组成的的实验探究


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案科目:初中化学 来源:2014-2015学年广西南宁市初三上学期期中考试化学试卷(解析版) 题型:选择题
在实验室用分解过氧化氢溶液的方法制取氧气,加入二氧化锰的目的是
A、使产生氧气的量增多 B.提高氧气的纯度
C.使其在常温下迅速分解放出氧气 D.使生成的氧气更干燥
查看答案和解析>>
科目:初中化学 来源:2014-2015学年福建省龙岩市分校初三上学期第三次阶段考试化学试卷(解析版) 题型:选择题
下列推理不正确的是
①燃烧过程中伴随着发光放热,所以有发光放热现象的变化一定是燃烧
②分子可以构成物质,所以物质一定是由分子构成的
③单质只含一种元素,所以含一种元素的物质一定是单质
④物理变化没有新物质生成,所以没有新物质生成的变化一定是物理变化
⑤氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物
A.①②③⑤ B.①②⑤ C.①③④ D.③⑤
查看答案和解析>>
科目:初中化学 来源:2014-2015学年福建省龙岩市初三上学期第三次单元考试化学试卷(解析版) 题型:填空题
(6分)在宏观、微观和符号之间建立联系是化学学科的特点。
(1)在水、铁和氯化钠三种物质中,由分子构成的是 。
(2)在符号①Fe3+ ②H2O2 ③SO42- 中,表示阳离子的是 ;①和③形成化合物的化学式是 。
(3)某密闭容器中物质变化过程的微观示意图如下:

①A、B、C中表示混合物的是 (填序号)。
②上述变化Ⅰ、Ⅱ和Ⅲ中,属于物理变化的是 。
③变化中“ ”和“
”和“ ”的质量比为 。
”的质量比为 。
查看答案和解析>>
科目:初中化学 来源:2014-2015学年福建省龙岩市初三上学期第三次单元考试化学试卷(解析版) 题型:选择题
下列关于“物质——用途——性质”的说法不正确的是
A.氧气——火箭发射——可燃性
B.干冰——制冷剂——升华吸热
C.氮气——食品防腐——常温下化学性质稳定
D.稀有气体——霓虹灯——通电能发出不同颜色的光
查看答案和解析>>
科目:初中化学 来源:2014-2015学年福建省龙岩市初三上学期第三次单元考试化学试卷(解析版) 题型:选择题
下列物质在氧气中燃烧,有大量白烟产生的是
A.硫 B.木炭 C.红磷 D.铁丝
查看答案和解析>>
科目:初中化学 来源:2014-2015学年安徽省蚌埠市初三上学期期中质量检测化学试卷(解析版) 题型:探究题
(11分)某校化学兴趣小组将用剩的过氧化氢溶液倒入放有生锈铁钉的废液缸中,发现产生了大量的气泡,经检验此气体为氧气。根据学过的知识初步判断,是生锈铁钉中的某种物质加快了过氧化氢的分解,那么究竟是哪种物质加快了过氧化氢的分解速率?请你参与他们的研究,分享和体验探究实验的快乐。
【猜想与假设】
甲同学:铁钉表面的氧化铁加快了H2O2的溶液分解。
乙同学:铁钉里的 加快了H2O2的溶液分解。
【设计方案和实验】完成下列表格
实验方案 | 实验现象 | 结论 |
方案一:向盛有10mL 5% H2O2溶液的试管中加入2g 氧化铁粉末,将一根带火星的木条放在试管口,观察现象。 | 甲同学结论成立。 | |
方案二:向盛有10mL 5% H2O2溶液的试管中加入 粉末,将一根带火星的木条放在试管口,观察现象。 | 无现象 | 乙同学结论 。 (填“成立”或“不成立”) |
【讨论交流】丙同学认为“方案一”只能说明Fe2O3加快了H2O2溶液的分解,并不能说Fe2O3就一定是催化剂。你是否支持丙同学的观点? ,如果要证明氧化铁是催化剂,就要设计一个实验来证明,这个实验的设计原理是 。
【拓展】
(1)实验证明Fe2O3粉末可以作为H2O2分解的催化剂。该反应的文字表达式
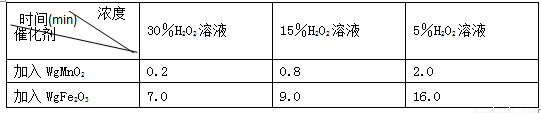
(2)下表是丙同学探究影响H2O2分解速率时所记录的部分数据,通过对数据分析,你能得出什么结论? 。
用足量等体积H2O2溶液制取相同体积O2所需的时间:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com