
分析 根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能共存,据此进行分析判断即可.
解答 解:A、NH4+、OH-两种离子能结合成氨气和水,不能大量共存,故选项错误;
B、某溶液中大量存在的离子仅有NH4+、Ca2+和X离子,NH4+、Ca2+均带正电荷;溶液中应含有阳离子和阴离子,NO3-带负电荷,能够和NH4+、Ca2+共存,符合要求,故选项正确;
C、某溶液中大量存在的离子仅有NH4+、Ca2+和X离子,NH4+、Ca2+均带正电荷;溶液中应含有阳离子和阴离子,Na+也带正电荷,不符合要求,故选项错误;
D、Cl-和NH4+、Ca2+不能结合成沉淀、气体或水,能大量共存.
故答案为:B;Cl-.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 高层住房着火时,立即打开所有门窗 | |
| B. | 煤气泄漏,立即打开排气扇电源开关 | |
| C. | 炒菜时油锅着火,立即浇水灭火 | |
| D. | 燃着的酒精灯不慎碰倒,立即用湿布盖灭 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
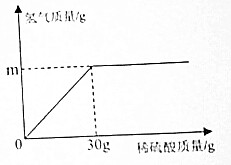 (1)实验室现有质量分数为98%(密度:1.84g/cm3)的浓硫酸,欲将这种浓硫酸稀释为19.6%的稀硫酸184g,需要这种浓硫酸体积为20mL;
(1)实验室现有质量分数为98%(密度:1.84g/cm3)的浓硫酸,欲将这种浓硫酸稀释为19.6%的稀硫酸184g,需要这种浓硫酸体积为20mL;查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
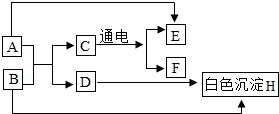 A-H是初中化学常见的物质,其相互转化关系如图所示,其中A是人体胃液中帮助消化的物质,B用于改良酸性土壤.
A-H是初中化学常见的物质,其相互转化关系如图所示,其中A是人体胃液中帮助消化的物质,B用于改良酸性土壤.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 某校化学性质在利用硫酸和氢氧化钠溶液探究酸碱中和反应时.利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示.下列说法正确的是A.
某校化学性质在利用硫酸和氢氧化钠溶液探究酸碱中和反应时.利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示.下列说法正确的是A.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 煅烧后固体中钙元素的质量分数减少 | |
| B. | 共生成1mol氧化钙 | |
| C. | 煅烧后固体中氧元素的质量不变 | |
| D. | 共生成16g二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com