
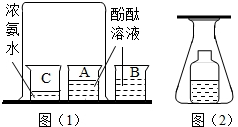
 以下是甲同学和乙同学设计的证明分子运动的实验:甲同学的实验如图(1)所示,图(2)是乙同学的实验,在锥形瓶中的小瓶里装着浓氨水,锥形瓶口用一张滤纸盖住,滤纸刚刚用酚酞溶液浸过.
以下是甲同学和乙同学设计的证明分子运动的实验:甲同学的实验如图(1)所示,图(2)是乙同学的实验,在锥形瓶中的小瓶里装着浓氨水,锥形瓶口用一张滤纸盖住,滤纸刚刚用酚酞溶液浸过.

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:初中化学 来源: 题型:阅读理解
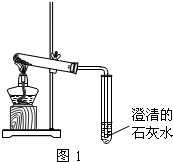 含钠元素、钙元素的化合物是初中化学的重要研究对象之一.
含钠元素、钙元素的化合物是初中化学的重要研究对象之一.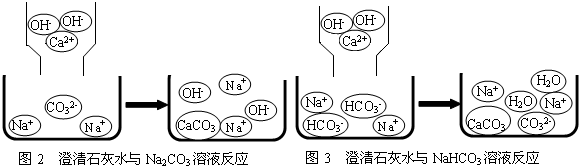
| 实验内容 | 实验现象 | 实验结论 |
| 方案一:取少量滤液加入试 管中,向其中 |
娇娇同学的猜想是正确的. 滤液中含有的两种溶质是 | |
| 方案二:取少量滤液加入试管中,向其中 |
 学们认为实验过程中产生的废液必须处理后再排放.请你对B试管中滤液的处理提出可行的建议
学们认为实验过程中产生的废液必须处理后再排放.请你对B试管中滤液的处理提出可行的建议查看答案和解析>>
科目:初中化学 来源:2012-2013学年北京市朝阳区中考二模化学试卷(解析版) 题型:探究题
化学小组用生石灰制取氢氧化钠固体,他们将生石灰放入烧杯中,加入碳酸钠溶液,充分反应后冷却、过滤、洗涤得到固体A和溶液B.请完成以下探究.
[查阅资料]NaOH、Ca(OH)2的溶解度
|
温度(℃) |
0 |
20 |
40 |
60 |
80 |
100 |
|
NaOH溶解度(g) |
42 |
109 |
129 |
174 |
314 |
347 |
|
Ca(OH)2溶解度(g) |
0.18 |
0.16 |
0.14 |
0.12 |
0.09 |
0.07 |
(1)固体A中的成分是什么?
[猜想与假设]
甲同学:
乙同学:CaCO3,Ca(OH)2
乙同学猜想可能含有的Ca(OH)2理由是 [实验与探究]甲、乙同学为了验证各自的猜想,分别进行了实验:
|
实验内容 |
实验现象 |
实验结论 |
|
甲同学:取少量固体于试管中,再加入稀盐酸. |
有气泡产生 |
自己的猜想正确 |
|
乙同学:取少量固体于试管中,加水充分振荡,过滤,向滤液中滴加 . |
溶液由无色变为红色 |
自己的猜想正确 |
[反思与评价]小组同学讨论后认为,甲同学的实验不能证明固体A的成分,理由是 结合甲、乙两同学的实验能证明乙同学的猜想正确,因此确定了固体A的成分.
(2)溶液B中溶质的成分是什么?
[猜想与假设]丙同学:NaOH、Na2CO3 丁同学:NaOH、Ca(OH)2戊同学:NaOH
[表达与交流]
①结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由是 ②同学们欲将溶液B加热浓缩,加热不久,溶液出现浑浊,只好停止加热,请解释加热时溶液出现浑浊的原因 ③同学们立即变换方案,向B溶液中加入 ,过滤,将滤液加热浓缩至饱和, 、过滤、洗涤、烘干得纯净的氢氧化钠固体.
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 含钠元素、钙元素的化合物是初中化学的重要研究对象之一.
含钠元素、钙元素的化合物是初中化学的重要研究对象之一.
| 实验内容 | 实验现象 | 实验结论 |
| 方案一:取少量滤液加入试 管中,向其中______ | ______ | 娇娇同学的猜想是正确的. 滤液中含有的两种溶质是 ______ |
| 方案二:取少量滤液加入试管中,向其中______ | ______ |
 学们认为实验过程中产生的废液必须处理后再排放.请你对B试管中滤液的处理提出可行的建议______
学们认为实验过程中产生的废液必须处理后再排放.请你对B试管中滤液的处理提出可行的建议______查看答案和解析>>
科目:初中化学 来源:2010年江苏省淮安实验中学中考化学模拟试卷(解析版) 题型:解答题
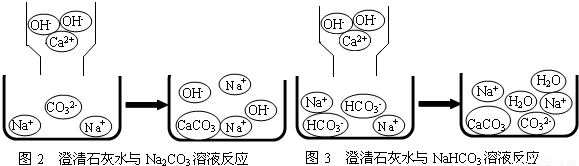
| 实验内容 | 实验现象 | 实验结论 |
| 方案一:取少量滤液加入试 管中,向其中______ | ______ | 娇娇同学的猜想是正确的. 滤液中含有的两种溶质是 ______ |
| 方案二:取少量滤液加入试管中,向其中______ | ______ |
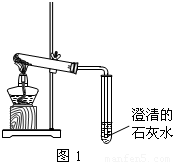
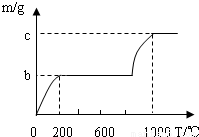
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com