解:(1)用加热高锰酸钾的方法制备氧气的发生装置的特点属于固体加热型的A装置;而要收集到干燥的氧气,则采用向上排空气法(D)收集,而不能采用排水法;
加热高锰酸钾产生锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO
4
K
2MnO
4+MnO
2+O
2↑;
检验集气瓶中氧气已集满的方法为:将带火星的木条放置在集气瓶口,如果能够复燃,说明氧气已集满;
(2)a是长颈漏斗;检验此套装置气密性的方法是:关闭弹簧夹,从长颈漏斗注入一定量的水使长颈漏斗中的液面高于试管内的液面,静止一段时间后,若看到长颈漏斗内液面没有下降,则表明装置气密性良好;
(3)图F是采用排水法测二氧化碳的体积,用量筒测量水的体积从而测二氧化碳的体积;二氧化碳能溶于水,所以要在水的上方放一层植物油,防止二氧化碳溶于水.排水法测气体体积的原理是利用排出水的体积和进入装置中的气体的体积相等的原理进行的,所以在没有二氧化碳生成时,盛水的集气瓶中压强和外界大气压是相等,当有二氧化碳气体生成时,集气瓶内气体压强增大,将水排出,所以油上方的空气对实验结果没有影响;
(4)解:A、因红磷能与空气中的氧气反应生成固态P
2O
5,固体生成物的体积对实验结果几乎没有影响,因此A正确;
B、因硫或木炭与氧气反应生成物都为气体,不能用于该实验,故B不正确.
C、红磷的量足,能耗尽氧气,当氧气耗尽后,反应停止,水位不会继续上升,故C不正确;
D、该实验中红磷只与空气中氧气反应,所以只能确定空气中有氧气,剩余气体的成分不能确定,因此D不正确.
故选A.
故答案为:(1)AD 2KMnO
4
K
2MnO
4+MnO
2+O
2↑ 将带火星的木条放置在集气瓶口,如果能够复燃,说明氧气已集满
(2)长颈漏斗 水 液面没有下降
(3)防止因CO
2 溶于水而引起体积测量结果不准确(偏小) 没有
(4)A
分析:(1)根据反应物的状态和反应条件选择发生装置,根据气体的溶解性和密度选择合适的收集方法;加热高锰酸钾产生锰酸钾、二氧化锰和氧气;验满氧气的方法是:将带火星的木条放置在集气瓶口,看木条能否复燃;
(2)熟练掌握常见的化学仪器名称及用途;检验此套装置气密性的方法是:“两孔变一孔法”,即:关闭弹簧夹,从长颈漏斗注入一定量的水使长颈漏斗中的液面高于试管内的液面,静止一段时间后,若看到长颈漏斗内液面没有下降,则表明装置气密性良好;
(3)根据实验目的及二氧化碳的水溶性进行分析植物油的作用,根据排水法测气体的体积的原理判断空气的影响;
(4)根据空气中氧气含量测定的原理分析:在密闭容器内消耗氧气,测量容器内气体体积的减少量确定氧气的含量.因此在选择消耗氧气的药品时,应考虑能与空气中的氧气反应而不与空气中的其他成分反应,生成物不能为气体;还应注意装置不漏气,药品的量要足,读数时温度要回到原来的温度等.
点评:本题主要考查学生对实验室制备氧气和二氧化碳的反应原理、发生装置的选择、收集装置的选择及有关气体体积测定方法的掌握情况.

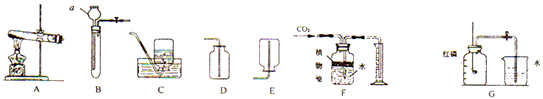
 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑; K2MnO4+MnO2+O2↑ 将带火星的木条放置在集气瓶口,如果能够复燃,说明氧气已集满
K2MnO4+MnO2+O2↑ 将带火星的木条放置在集气瓶口,如果能够复燃,说明氧气已集满

 (2013?顺义区二模)如图为实验室常用的实验装置,回答有关问题.
(2013?顺义区二模)如图为实验室常用的实验装置,回答有关问题.


