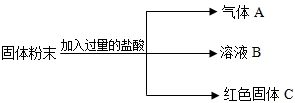
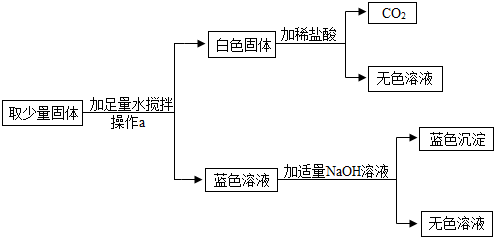
有一包固体粉末,可能由KNO3,,Ba(NO3)2,CuCl2,Na2CO3,K2SO4中的一种或几种组成,做如下实验:
①取一定量的固体粉末,加入足量水中搅拌,静置,得到白色沉淀和无色溶液.
②取白色沉淀,加入过量的盐酸后,沉淀完全溶解,且有无色气体产生.
从实验可以判断出:
该粉末中一定含有______,一定不含有______.
【答案】分析:根据实验现象进行分析,取粉末溶于水,得到白色沉淀和无色溶液,则一定不含氯化铜,白色沉淀可能是硝酸钡与碳酸钠反应生成的碳酸钡,也可能是硝酸钡与硫酸钾反应生成的硫酸钡沉淀,也可能两种沉淀都有,向白色沉淀加入过量的盐酸后,沉淀完全溶解,且有无色气体产生,则沉淀中不含有硫酸钡,含有碳酸钡,要生成碳酸钡,一定含有硝酸钡和碳酸钠,无硫酸钡沉淀,则一定不含有硫酸钾,硝酸钾是否含有无法确定.
解答:解:①取粉末溶于水,得到白色沉淀和无色溶液,则一定不含氯化铜,白色沉淀可能是硝酸钡与碳酸钠反应生成的碳酸钡,也可能是硝酸钡与硫酸钾反应生成的硫酸钡沉淀,也可能两种沉淀都有;
②向白色沉淀加入过量的盐酸后,沉淀完全溶解,且有无色气体产生,则沉淀中不含有硫酸钡,含有碳酸钡,要生成碳酸钡,一定含有硝酸钡和碳酸钠,无硫酸钡沉淀,则一定不含有硫酸钾,硝酸钾是否含有无法确定;
故答案为:Ba(NO3)2、Na2CO3 ; CuCl2、K2SO4;
点评:此题为文字叙述型物质推断题,完成此题,可以依据题干提供的实验现象,结合物质间的反应进行,要求同学们熟练掌握物质间的反应现象,以便灵活应用.