
����Ŀ��ˮ֮�ʡ�
(1)ͨ����ͼ1���ˮʵ�飬֤��ˮ����___________Ԫ����ɣ�����������������__________�� ������һ���缫����5 mL����ʱ����һ�缫�������������������_____________mL.
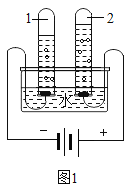
(2)����ɽ��������С�����δ���һƿɽȪˮ��ȡ��������������ˮ�������϶���ĭ�����ɽȪˮ����_____________ (�� ��Ӳˮ��������ˮ��)��
(3)����ˮ�ڴ��������������ϸ�����ڼ������ø�ˮ֮ǰ����_____________����������
(4)�������� �dz����Ļ���ҩ�Ϊ��ɫ�����壬�۵�Ϊ48��C���е�100��C����ͼ2װ�ö��������������ۻ�������ˮ����Ҫ������____________(����ţ� �ɶ�ѡ)��
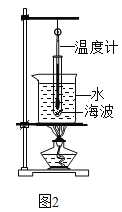
A ��ʵ����ˮ�����¶ȵ�����
B ˮ��Ѹ�ټӿ������������ۻ�
C ʹ�����������ȸ�����
���𰸡��⡢�� ���� 10��2.5 ��ˮ ��� A��C
��������
��1��ˮ�ĵ�⣬������������������˵��ˮ������Ԫ�غ���Ԫ����ɡ��������������������������һ������ˮ��������һ���缫����5mL����ʱ�����õ缫������������һ�缫�����������������10mL�����õ缫�Ǹ���������һ�缫�����������������2.5mL��
��2���÷���ˮ��������Ӳˮ����ˮ����ĭ�������ˮ����ĭ�ٵ���Ӳˮ��ȡ��������������ˮ�������϶���ĭ�����ɽȪˮ������ˮ��
��3������ˮ�ڴ�������д���ϸ����Ⱦ�������ڼ������ø�ˮ֮ǰ���Լ�����У�����Ч��ɱ��ϸ����
��4��A����ʵ����ˮ�����¶ȵ����ã�����ȷ��
B��ˮ����Ѹ�ټӿ조���������ۻ����ʴ���
C��ʹ�����������ȸ����ȣ�����ȷ��
���A��C��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��A�ǽ��������B�ǽ������ʣ�C�ǻ�ɫ��Һ��D��dz��ɫ��Һ��E�Ǻ��ɫ��������Ӧ��������F��������ˮ�����Ļ��Ϸ�Ӧ����ش��������⣺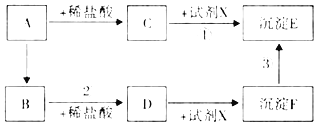
��1��д��C�Ļ�ѧʽ_____��
��2����ѧ��Ӧ�ٵĻ���������_____��
��3��д����Ӧ�ں͢۵Ļ�ѧ����ʽ����_____����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��H�dz��л�ѧ���������ʣ����ת����ϵ��ͼ��ʾ������A������θҺ�а������������ʣ�B ���ڸ�������������
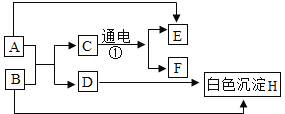
��1��D�Ļ�ѧʽΪ_______��
��2��Aת��ΪE �Ļ�ѧ����ʽ___________________��
��3��ָ��Aת��ΪE��Ӧ�Ļ�����Ӧ����_______��
��4��ָ������ H ��һ����;_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʦ��ָ���£�С����С��������ͼ1��ʾװ�ö���������������������˵�̽��ѧϰ��
����:
������ص��۵�ԼΪ356��C���������̵ķֽ��¶�ԼΪ535��C���þƾ��Ƹ����ʼ���,�������ʵ��¶�һ��ԼΪ400��C����;
����ͬ�����ָ����غͶ������̻�����У�����غͶ������̵�������;
������طֽ�ʱ���������������Ũ�����¶ȵı仯ʾ��ͼ(ͼ2)����ͬ���ʱ����Ũ�����¶ȵı仯ʾ��ͼ(ͼ3)���¡�
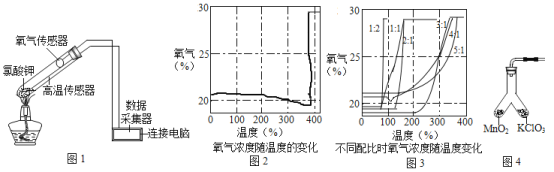
��ش���������:
��1������ͼ2,����طֽ��¶�_____(������������������������������)���۵㡣
��2������ͼ2,������طֽ�ǰ���������������Ũ�Ƚ��͵Ŀ���ԭ����_________��
��3������ͼ3,����طֽ��¶���������ȱ仯�Ĺ�����_______��
��4��Ϊ֤ʵ�������̵Ĵ�����,С��������ͼ4װ�ý������±���ʾ��ʵ��:
���� | ʵ����� | ʵ������ | ʵ����� |
�� | ���װ�������� | ||
�� | �ֱ�����Y"�ι�����֧���м��������������̺�����أ�������Ƥ���� | û���������� | |
�� | �ֱ��þƾ����Ⱥ���ȶ�����������أ��ô�����ľ�����ڵ��ܿڡ� | �������֧�ܣ��ɹ۲� ��________�������Ҳ�֧�ܣ��ɹ۲쵽________�� | �����������Ȳ��ֽ�;��������Ƚϳ�ʱ���ֽ⡣ |
�� | ��ȴ��, ����Y�� �ι����֧���в��ֶ������̻����Ҳ�֧��:�У�����Y���ιܼ��ȣ��ô�����ľ�����ڵ��ܿڡ� | ����ʱ����벽����ľ���ܿ츴ȼ | �û�ѧ��ʽ��ʾ_______�� |
��ش�:
��������������
�ڲ���IV�У����������̻����Ҳ�֧�������ȵ�������еIJ���������_________��
��С����Ϊ���ݲ���IV��ʵ���������˵����������������طֽ�Ĵ�������С����ͬ�����Ĺ۵㣬С����Ϊ����֤���ڴ˷�Ӧ�ж������̵�______��_________���䡣��������ʦ��ָ���£�С��������ʵ�鷽��,������֤���Լ��Ľ��ۡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС����������ȡ�����Ĵ���չ��̽������ش���������:
̽��һ:��������������С�Դ�Ч����Ӱ��

ȡ���ݵ���������أ��ֱ�����������������С��ͬ�Ķ������̽��м��ȣ��ô�������ù��������(��Ӧ��ʣ����������뷴Ӧǰ��������֮��)����ͼ:
(1)���������������������������ȡ�����Ļ�ѧ����ʽΪ_____________��
(2)�������ϵ�֪��������Ӧ���¶�Խ�ͣ���Ч��Խ�á�������ͼ,������طֽ��Ч�����õ���_____________����Ч�����õ�ԭ�������_____________��
̽����:������������������Դ�Ч����Ӱ��
ͬѧ���������ʵ�鷽��:
��� | ���������/g | ���� | ��������/g | �ռ�VmL���� ����ʱ��/s |
ʵ��1 | 5 | 171 | ||
ʵ��2 | 5 | �������� | 0.25 | 79 |
ʵ��3 | 5 | �������� | 0.5 | 49 |
ʵ��4 | 5 | �������� | 2.5 | 93 |
ʵ��5 | 5 | ������ | 0.5 | 58 |
ʵ��6 | 5 | �Ȼ��� | 0.5 | 154 |
(3)�����������ִ����У���Ч����õ���_____________��
(4)��������������ص�������Ϊ_____________ʱ����Ч����á�
(5)�Ȼ���_____________(����������������)�����á�ά�ּ����������䣬��ʵ��1�ټ����ռ�VmL����������ʱ����������171s,ԭ����_____________��
̽����:�������������ڷ�Ӧǰ��ı仯
ͬѧ�Ƿ���ÿ��������غͶ���������ȡ�����������ڲ�жװ��ʱ�����ŵ��̼�����ζ�����ǽ����Ⱥ�ʣ������еĶ������̷��벢������������������С�ڼ���ǰ�������̵��������������Ϻ��֣�һ����Ϊ��������غͶ������̻����ķ�Ӧ��������:
��1��: ![]() (����Cl2�д̼�����ζ)
(����Cl2�д̼�����ζ)
��2��: ![]()
��3��: ![]()
(6)��3����Ӧ����Ԫ�ػ��ϼ۱仯Ϊ_____��________��
(7)��Ӧ��ʣ������ж�����������С�ڷ�Ӧǰ��������ԭ�������_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����Ȼ����һ����̼ѭ�����̣����ڸù���������ȷ���ǣ�������
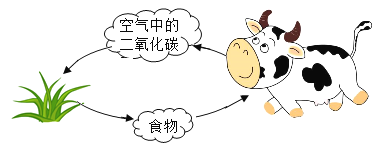
A. ��ֲ��ĺ�������Ϊ��������ṩ�����еĶ�����̼
B. ֲ��ֻ��ͨ��������ý������е�̼Ԫ��ת�Ƶ�����
C. ֲ�����ڵ��л���ֻ��ͨ�������ĺ�������ת��Ϊ������̼
D. �ҹ������Ķ��죬������Ҷ���䣬�ᵼ�´����еĶ�����̼��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������CaCl2�Ļ����Һ����������ε���Na2CO3��Һ�����ɳ������������Na2CO3��Һ�����ı仯��ϵ����ͼ��ʾ������˵����ȷ����
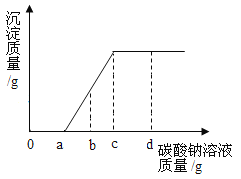
A.����a��ʱ����Һ�з�ӦΪ![]()
B.����b��ʱ����Һ�к�HCl��NaCl��������
C.����c��ʱ����Һ������������ԭ�����Һ������������
D.����d��ʱ����Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ij�ܱ����������ʱ仯���̵���ʾ��ͼ��
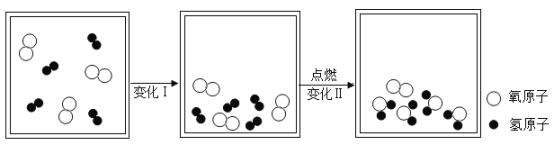
��1���仯������______�仯��ѡ��������������ѧ������ԭ����__________�����۵ĽǶȽ��ͣ���
��2���������������������_______������ţ��ٻ����ڴ�����۵��ʡ��ܻ�������������
��3���仯���Ļ�ѧ��Ӧ����ʽΪ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ú�ˮ��ȡ���εĹ�������ͼ��ʾ���ش��й����⡣
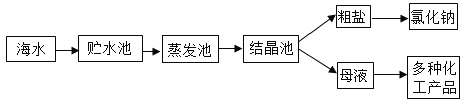
��1��һ�������ĺ�ˮ��ͨ����ˮ�����뵽�����أ���û������ᾧ��֮ǰ�����������У����������Ȼ��Ƶ�������__________����������������������������С������
��2�������к��е���������������ʵ���������ͨ���ܽ⡢���ˡ������Ȳ�������ȥ������Щ�����ж����õ�������______________��
��3�����Ȼ��ƹ�������100g��������Ϊ20%���Ȼ�����Һ��
������ʱ���漰����ʵ�鲽�裺A.��������ȡ B.���� C.�ܽ� D.װƿ����ǩ������ȷ��ʵ�鲽��˳����___________________________������ĸ����
��ȡ����õ�50g��������Ϊ20%���Ȼ�����Һ�����������Ϊ5%���Ȼ�����Һ����Ҫ�ټ�ˮ��������___________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com