生活处处皆化学.
(1)生活中的燃烧
①着火点比较:蜂窝煤
>
>
小木条(填“>”、“<”或“=”).生煤炉过程中,不断扇入空气目的是
与氧气充分接触
与氧气充分接触
,煤不完全燃烧产生一种有毒气体的化学式是
CO
CO
;
②用水灭火的原理是
水蒸发吸热,使温度降低到着火点以下
水蒸发吸热,使温度降低到着火点以下
,新型水成膜泡沫灭火剂扑灭油类火灾时,析出的液体和泡沫在油面上铺展形成一层水膜,进而灭火,原理是
隔绝氧气
隔绝氧气
.
(2)金属在生活中用途广泛
①如图1下列生活用品,主要是由金属材料制成的是
AC
AC
;

品名:504双吸剂
成分:铁粉、NaCl、炭粉CaO等 |
图3
②用铁锅烹饪食物时,会有少量铁屑在胃部转化为可被吸收的Fe
2+,反应的化学方程式为
Fe+2HCl═FeCl2+H2↑
Fe+2HCl═FeCl2+H2↑
,是
置换
置换
反应(填基本反应类型).
③用铝箔包装药物,主要利用了铝的
延展
延展
性;
④铜具有很好的
导电
导电
性,故可作导线.近代湿法冶金的先驱是指
Fe+CuSO4═FeSO4+Cu
Fe+CuSO4═FeSO4+Cu
(填化学方程式),铜和空气中的O
2、H
2O及
CO2
CO2
会生成铜锈[Cu
2(OH)
2CO
3],反应的化学方程式是
2Cu+O2+H2O+CO2═Cu2(OH)2CO3
2Cu+O2+H2O+CO2═Cu2(OH)2CO3
.
(3)生活中的水和溶液
①处理自然水时,常用的混凝剂是
明矾
明矾
(填名称).二氧化氯是一种新型的消毒剂,其化学式为
ClO2
ClO2
;
②欲配制500mL 0.9%的生理盐水(密度为1.0g/mL),需要NaCl的质量为
4.5
4.5
g;配制过程中,玻璃棒的作用是
搅拌,加快溶解
搅拌,加快溶解
,称量NaCl时,若将砝码放在左盘(1g以下用游码),其他操作均正确,则所配溶液中溶质质量分数将
<
<
0.9%(填“>”、“<”或“=”)
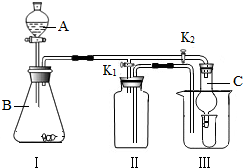
③图2是净化河水的简易装置,下列说法正确的是
D
D
;
A.净化后的水是纯净物 B.此装置能对水杀菌消毒
C.此装置能把硬水变为软水 D.活性炭能吸附水中的色素及异味
④KNO
3可用作配制无土栽培营养液,下表提供了KNO
3在不同温度时的溶解度:
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
| 溶解度/g |
13.3 |
31.6 |
63.9 |
110 |
169 |
a.从上表可总结出KNO
3的溶解度随温度变化的趋势是
随温度升高而增加
随温度升高而增加
;
b.20℃时,将20gKNO
3加入50g水中充分溶解,所得溶液的质量为
65.8
65.8
g;
c.现有60℃时的KNO
3饱和溶液210g,降温至20℃,会析出KNO
378.4
78.4
g;
(4)食品包装学问大
①我区特产--嘶马羊耳采用真空包装,延长了食品的保质期,原理是
隔绝氧气,杜绝缓慢氧化
隔绝氧气,杜绝缓慢氧化
;
②将N
2充入包装袋内做保护气,是因为N
2的化学性质
稳定
稳定
(填“活泼”或“稳定”);
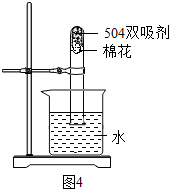
③图3是“504双吸剂”的标签,请问答下列问题:
a.其中至少含有
2
2
种单质;
b.取少量双吸剂加入蒸馏水中,振荡后静置,测得上层清液的pH=9,若用pH试纸测定,具体操作是
用玻璃棒蘸取一滴上层清液,滴在pH试纸上,待颜色不再变化时和标准比色卡对照,读数
用玻璃棒蘸取一滴上层清液,滴在pH试纸上,待颜色不再变化时和标准比色卡对照,读数
.通入CO
2后,上层清液变浑浊,写出上述变化的化学方程式
H2O+CaO═Ca(OH)2
H2O+CaO═Ca(OH)2
、
Ca(OH)2+CO2═CaCO3↓+H2O
Ca(OH)2+CO2═CaCO3↓+H2O
;
c.为测定此双吸剂的使用效果,取足量双吸剂做了如图4所示的实验,一段时间后,进入试管中水的体积
>
>
21%(填“>”、“<”或“=”),理由是
此双吸剂能同时吸收空气中的O2和CO2,也可吸收H2O
此双吸剂能同时吸收空气中的O2和CO2,也可吸收H2O
;
d.部分失效的双吸剂中,有红棕色固体,其主要是
氧化铁
氧化铁
;
e.此双吸剂中,NaCl的作用可能是
加快双吸剂中铁粉吸收O2的速率
加快双吸剂中铁粉吸收O2的速率
.

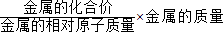 ,假设6.5g全部为铁,铁与盐酸反应时铁为+2价、铁的相对原子质量为56,可计算产生氢气的质量=
,假设6.5g全部为铁,铁与盐酸反应时铁为+2价、铁的相对原子质量为56,可计算产生氢气的质量=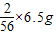 ≈0.23g>0.19g;则铁中应含有不与酸发生反应或虽与酸反应但等质量金属产生氢气的量小于0.19g.
≈0.23g>0.19g;则铁中应含有不与酸发生反应或虽与酸反应但等质量金属产生氢气的量小于0.19g.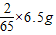 =0.2g>0.19g,故所含杂质不可能是锌;故不选A;
=0.2g>0.19g,故所含杂质不可能是锌;故不选A;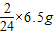 ≈0.54g2g>0.19g,故所含杂质不可能是镁;故不选B;
≈0.54g2g>0.19g,故所含杂质不可能是镁;故不选B;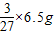 ≈0.72g2g>0.19g,故所含杂质不可能是铝;故不选C;
≈0.72g2g>0.19g,故所含杂质不可能是铝;故不选C;

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案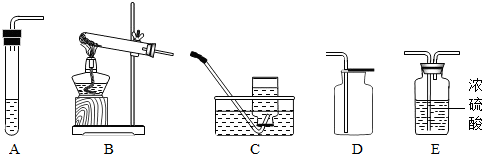


 甲同学用一氧化碳还原铁的氧化物,取不同质量的铁的氧化物进行实验,所得到的数据如下表所示:
甲同学用一氧化碳还原铁的氧化物,取不同质量的铁的氧化物进行实验,所得到的数据如下表所示: 【醋与人体健康】
【醋与人体健康】