
【题目】根据实验,请回答下列问题。

(1)实验一中,若玻璃管太长,则不易观察到蜡蒸汽燃烧,其原因是_____。
(2)实验二中,玻璃棒起_____作用,实验结束后,发现烧杯中的液体仍然浑浊,可能原因是_____。(写一条即可)
(3)实验三中,在保鲜袋内加入少量酒精,排出袋内空气后封闭,放在热水中,发现保鲜袋迅速鼓起,请从微观角度解释产生上述现象的原因_____。
(4)实验四中白磷在锥形瓶中燃烧时,常常导致瓶塞被冲开,实验失败。导致瓶塞被冲开的原因是_____;为了防止瓶塞被冲开,请你将实验进行改进,改进的措施为_____。
【答案】蜡蒸汽冷凝在玻璃管中 引流 滤纸破损或倾倒的液体液面高于滤纸边缘(答案合理即可) 酒精分子受热分子间隔变大 白磷燃烧时放出的热使锥形瓶内气体膨胀,瓶内压强大于外部大气压,冲开瓶塞 将锥形瓶上单孔塞中的玻璃棒改为玻璃管,在玻璃管的外端扎上一个气球(答案合理即可)
【解析】
1)实验一中,若玻璃管太长,则不易观察到蜡蒸汽燃烧,其原因是:蜡蒸汽冷凝在玻璃管中,不易点燃;
(2)实验二中,玻璃棒起引流作用,防止液体飞溅,实验结束后,发现烧杯中的液体仍然浑浊,可能原因是:滤纸破损或倾倒的液体液面高于滤纸边缘;
(3)实验三中,在保鲜袋内加入少量酒精,排出袋内空气后封闭,放在热水中,发现保鲜袋迅速鼓起,微观角度解释产生上述现象的原因:温度升高,酒精分子受热分子间隔变大;
(4)实验四中白磷在锥形瓶中燃烧时,常常导致瓶塞被冲开,实验失败。导致瓶塞被冲开的原因是:白磷燃烧时放出的热使瓶内气体膨胀,锥形瓶内压强大于外部大气压,冲开瓶塞 ;为了防止瓶塞被冲开,改进的措施为:将锥形瓶上单孔塞中的玻璃棒改为玻璃管,在玻璃管的外端扎上一个气球。


科目:初中化学 来源: 题型:
【题目】追寻化学家的足迹,一起了解空气的发现史。
(1)舍勒是最早制得氧气的化学家之一,他获得氧气的方法主要有以下两种:
a.加热分解硝酸钾、氧化汞、碳酸银等
b.用二氧化锰与浓硫酸加热:2 MnO2 + 2 H2SO4(浓)![]() 2 MnSO4 + 2 X + O2↑
2 MnSO4 + 2 X + O2↑
①a 中反应物均可制得氧气,是因为它们组成的共同点:_____;
②b 中物质 X 化学式为_____;
(2)舍勒由于受“燃素说”的影响(即认为一切可以燃烧的物质都是由灰和“燃素”组 成的,物质燃烧后剩下的是灰,而燃素本身变成了光和热,散逸到空中去了),导 致“氧气”从他的鼻尖下溜走。化学家拉瓦锡结合大量实验事实,否定了“燃素 说”认为的“物质燃烧后质量应当减轻”的观点,真正发现了氧气。
①写出铁丝在氧气中燃烧的主要现象是_____,写出反应的化学 方程式:_____。
②以铁燃烧的事实,指出上述“燃素说”的谬误:_____。
(3)拉瓦锡用定量的方法研究了空气的成分(实验装置如图所示)。该实验中选择使用 汞的优点有_____。(填标号)
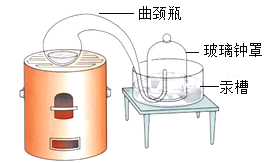
A 实验过程中没有污染
B 在汞槽中起到液封的作用
C 生成的化合物加热分解又能得到汞和氧气
D 能将密闭装置内空气中的氧气几乎耗尽
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了使同学们掌握酸根离子的检验方法,老师提供了一包白色固体,可能是碳酸钠、硫酸钠、氯化钠中的一种或几种。请你和同学们一起通过实验的方法探究白色固体的成分。
(提出问题)如何确定白色固体的成分?
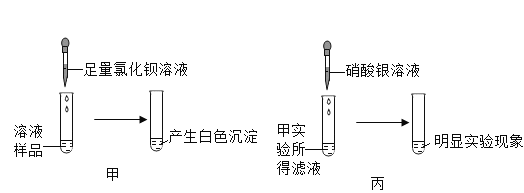
(实验探究)甲同学取少量白色固体配成溶液,取溶液样品,实验如图所示,由此他得出实验结论:白色固体中一定含有硫酸钠。
(收集证据)他得出此结论的理由是_______________(用化学方程式解释)。
(继续探究)乙同学取甲同学实验所得白色沉淀于试管中,向其中加入_________________,观察到白色固体表面冒气泡固体逐渐减少至消失,于是得出实验结论:原白色固体中一定含有__________(填化学式,下同),一定不含___________,据此可知甲同学的实验结论不正确。白色固体中是否含有氯化钠呢?丙同学取甲同学实验所得滤液,向其中滴加的酸银溶察到明显的实验现象,于是得出实验结论:白色固体中含有氯化钠。请你评价丙同学的及结论_______________。
(反思与实践)经研究,同学们对实验进行了适当的调经和改进,最终确定了白色固体的成分是碳酸钠和氯化钠。
(归纳与总结)由上述探究可知:如果我们取一次样品先后鉴别几种物质,在鉴别第一种物质时,要注意所加试剂不能____________(填一点)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类发现二氧化碳经历了多个世纪,下列是艾杯程中的部分资料。
资料一:1630年,比利时化学家海尔蒙特发现在一些洞穴中的地面附近,有一种能使燃着的蜡烛熄灭的气体,后来被证实是CO2。
(1)根据海尔蒙特的发现,可推测出二氧化碳具有的性质是_____。
资料二:1754年,英国化学家布莱克将石灰石煅烧首次制得CO2,并详细研究了“石灰石→生石灰→熟石灰→石灰石”的相互转化过程。
(2)煅烧石灰石的化学方程式为_____,所属的基本反应类型是_____反应。
资料三:1766年,英国化学家卡文迪许通过实验测得:室温下1体积水大约能溶解1体积二氧化碳气体。
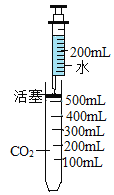
(3)如图,在带有可自由移动的活塞的容器中充满500mLCO2气体,用注射器缓慢注入200mL水,边注入边振荡。①充分振荡后,活塞停留在_____mL刻度处。②取少量量容器中的液体,滴加紫色石蕊试液,现象为_____。③将②所得的溶液加热至沸腾,发生反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“宏观辨识与微观探析”’是化学学科核心素养之一,化学学习要让学生既能够“见微知著”,也能够“见著知微”。金属钠在氯气中燃烧生成氯化钠,如图为氯化钠形成的示意图。
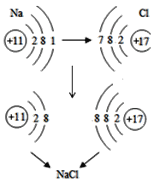
根据所给信息,请回答:
(1)钠原子的核外电子层数是_____,在化学反应中易_____(填“得到”或“失去”)电子。
(2)元素的化学性质主要是由原子的_____决定的。
(3)化学反应前后,氯元素的化合价为_____。
(4)构成氯化钠的离子是_____(填微粒符号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲和乙在一定条件下反应生成丙和丁。结合微观示意图分析,下列结论正确的是
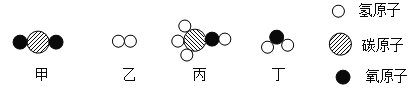
A.丙的相对分子质量为24
B.发生反应的甲和乙的质量比为22:3
C.反应前后分子总数不变
D.生成的丙和丁的分子个数比为2:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明发现他戴的铜质眼镜架表面变绿了,经过咨询老师知道是生成了铜锈。小明和实验小组的同学决定设计并进行实验,探究铜锈的组成和铜生锈的条件。
探究1:铜锈由哪些元素组成?
(查阅资料)铜锈受热易分解
(进行实验)利用下图所示装置对铜锈进行加热,观察到试管口有水珠生成,烧杯中澄清石灰水变浑浊,绿色固体变为黑色。
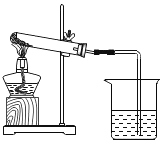
根据以上现象分析,铜锈中一定含有的元素:Cu和_____。
探究2:铜发生锈蚀的条件是什么?
(猜想与假设)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关
(进行实验)实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
现象 | 无明显现象 | 无明显现象 | 铜丝表面有绿色物质 | 无明显现象 | 无明显现象 |
(解释与结论)
(1)实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是_____。
(2)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是_____(填编号)。
(3)对比实验②和③,得出的结论是_____。
(4)为验证猜想,请在图中将实验⑤补充完整_____。
(5)由上述实验可推知,铜生锈的条件是_____。
(反思与评价)
(6)对实验进行反思后,同学们认为实验_____可以不用进行。
(7)根据实验结论,请你写出一种防止铜发生锈蚀的方法_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学探究过量的炭粉与Fe2O3在高温条件下反应的气体产物成分。探究过程如下:
(提出假设)气体产物是CO2。
(查阅资料)①氮气不能与炭粉及Fe2O3反应。
②高温下可以发生下列反应: ![]()
(设计方案)将一定量Fe2O3在隔绝空气的环境下与过量炭粉充分反应,用实验中测得的有关物质的质量,进行分析、判断。
(进行实验)用如图所示装置进行实验。首先称得玻璃管C的质量为48.48 g,再称取2.40 g Fe2O3和1.50 g炭粉,加到玻璃管C中。连接好装置,通一段时间氮气,再夹紧弹簧夹T,点燃酒精喷灯加热。待玻璃管C中固体质量不再变化时,称得玻璃管C与残留固体共51.30 g。

(问题分析)
(1)用酒精喷灯而不用酒精灯的目的是___________。
(2)加热前先通一段时间氮气的目的是___________。
(3)尾气处理的方法是___________。
(4)若Fe2O3与炭粉反应的气体产物全部是CO2. 求2.40 g Fe2O3完全反应时生成CO2的质量________。(写出计算过程)
(5)根据实验数据计算,实验中实际获得气体质量为________。
(6)结论:原假设_________(填“能”或“不能”)成立,理由是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过一个学期的化学学习,同学们初步掌握了实验室制取气体的知识和技能,请完成下列实验内容。
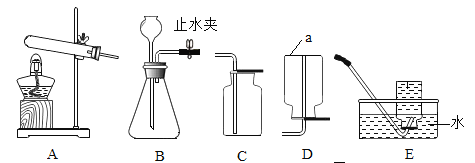
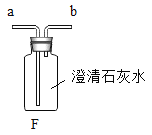
(1)写出仪器a的名称_________。
(2)甲同学选择装置A和E制取氧气,发生反应的化学方程式是_______________,他还能选择装置_________(填字母序号,下同)收集氧气。
(3)乙同学选择装置B和C制取二氧化碳气体,从长颈漏斗中加入的药品是_________。用装置_________检验产生的二氧化碳气体,检验的原理是________________。(用化学方程式表示)
(4)实验室常用锌粒和稀硫酸在常温下反应制取氢气,应选择的发生装置是_________,选择的依据是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com