
分析 (1)根据发生装置选择反应的原理和药品.根据气体密度和溶解性选择发生装置;
(2)根据二氧化碳密度大,不燃烧、不支持燃烧解答;
(3)根据电解水的实验解答;
(4)根据镁条在二氧化碳中燃烧生成氧化镁和碳下化学方程式;
(5)铜在加热的条件下转化为氧化铜;将铜丝绕成螺旋状,增大了与氧气的接触面积;根据改进后的装置的特点来分析.
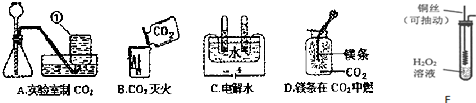
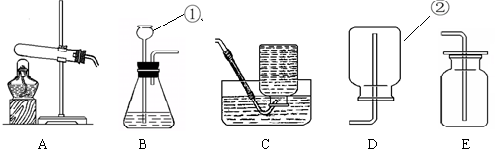
解答 解:(1)仪器①名称为集气瓶;实验室制取二氧化碳所用药品是大理石(或石灰石)和稀盐酸,二氧化碳密度大于空气,能溶于水,故只能用向上排空气法收集,图中的收集方法错误;该装置可以用来制取氧气,如果用双氧水和二氧化锰制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)把二氧化碳倒入梯形蜡烛的烧杯中观察到的现象是蜡烛由下到上逐渐熄灭;
(3)电解水,正氧负氢,故正极产生的是氧气,该实验证明了水是由氢元素和氧元素组成的;
(4)镁条在空气中点燃后再放入充满CO2的集气瓶中,燃烧生成氧化镁和碳,化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(5)将铜丝灼烧,铜与氧气反应生成氧化铜,化学方程式为:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;
①将铜丝绕成螺旋状,增大了与反应物的接触面积,加快了反应的速率;
②改进后的装置,通过抽动铜丝来控制反应的发生和停止.
故答案为:
(1)集气瓶,大理石(或石灰石)和稀盐酸,收集方法错误,是,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)蜡烛由下到上逐渐熄灭;
(3)O2,氢元素和氧元素;
(4)2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(5)灼烧;2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;
①B;②可随时控制反应的进行.
点评 本考点属于新信息筛选题,主要考查了通过实验现象分析物质的性质,以及质量守恒定律的应用,方程式的书写,能较好考查学生分析、解决问题的能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 物质都是由分子构成的 | |
| B. | 分子间没有空隙 | |
| C. | 原子是化学变化中不能再分的微粒 | |
| D. | 在化学反应前后,分子的种类和数目都保持不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 煤炉火上放一盆水,就能防止一氧化碳中毒 | |
| B. | 用生石灰固体来除去二氧化碳中的水蒸气 | |
| C. | 用燃烧的小木条放入集气瓶内来检验二氧化碳是否集满 | |
| D. | 用灼烧闻气味的方法区分羊毛线和棉线 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 金属与金属矿物
金属与金属矿物查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com