

分析 (1)根据常见的化学仪器的名称进行分析解答.
(2)根据实验室中制取二氧化碳的反应原理和反应条件来选择反应的发生装置,检验二氧化碳应用澄清的石灰水,进行分析解答.
(3)根据氧气不易溶于水,密度比空气的大,进行分析解答.
(4)实验室常用加热NH4Cl与Ca(OH)2混合物的方法来制取氨气,氨气的密度比空气小,极其溶于水,进行分析解答.
解答 解:(1)仪器X是铁架台;仪器Y是集气瓶.
(2)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液常温型,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.所以应该选择装置②来制取二氧化碳气体;常用澄清的石灰水检验二氧化碳气体,故检验二氧化碳的装置应选用装置⑥.
(3)氧气不易溶于水,密度比空气的大,能用排水法、向上排空气法收集,即收集装置是④或⑤.
(4)实验室常用加热NH4Cl与Ca(OH)2混合物的方法来制取氨气,属于固体加热型,应该选用的发生装置是①;氨气的密度比空气小,极其溶于水,可选用向下排空气法收集,故收集装置为③.
故答案为:(1)铁架台;集气瓶;(2)②;CaCO3+2HCl=CaCl2+H2O+CO2↑;⑥;(3)④或⑤;(4)①和③.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:初中化学 来源: 题型:选择题

| A. | 甲实验试管口向下倾斜可防止氢气逸出 | |
| B. | 乙实验只能通过澄清石灰水是否变浑浊判断反应是否发生 | |
| C. | 甲、乙两实验中,都应先通入气体,再使试管、玻璃管均匀受热,以防止发生爆炸 | |
| D. | 甲、乙两实验中,氢气和一氧化碳都将氧化铜变成游离态的铜,都发生了置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
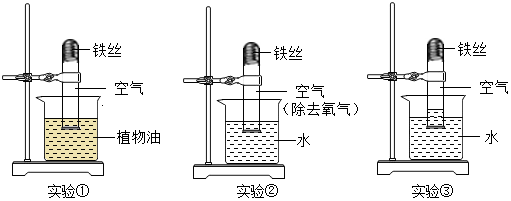
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.| 操作步骤 | 实验现象 | 实验结论 |
| 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口 | 试管中有气体产生,湿润的红色石蕊试纸变蓝 | 黄色固体为Mg3N2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 根据如图的信息判断,下列说法中不正确的是( )
根据如图的信息判断,下列说法中不正确的是( )| A. | 钛属于金属元素 | |
| B. | 钛原子核内有22个中子 | |
| C. | 在TiO2中,钛的化合价是+4价 | |
| D. | 钛子原核内质子数与中子数之和为48 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
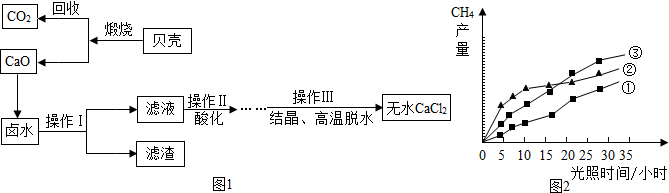
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
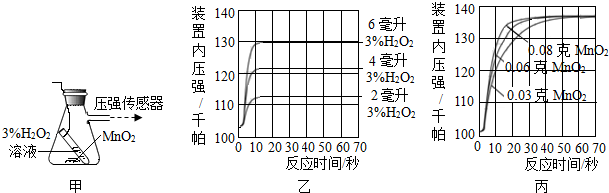

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 过滤能除去天然水中所有的杂质 | |
| B. | 将活性炭放入硬水中可使其软化 | |
| C. | 工业废水要经过处理后再排放 | |
| D. | 过量使用农药、化肥不会造成水体污染 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com