
| A、10 | B、14.2 |
| C、17.5 | D、9.8 |
| 73 |
| 7.3g |
| 2 |
| y |
| 100 |
| x |
| 56 |
| 9.8 |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
| A、饱和石灰水(CO2) |
| B、稀硫酸(氯化钡) |
| C、稀盐酸(氢氧化钠) |
| D、氢氧化钠溶液(硫酸铜) |
查看答案和解析>>
科目:初中化学 来源: 题型:
 甲乙小组按图1所示实验探究蜡烛的燃烧产物,获得了不同的实验现象.
甲乙小组按图1所示实验探究蜡烛的燃烧产物,获得了不同的实验现象.| 实验操作 | 实验现象 | |
| 甲组 | 取少量该黑色固体于a中,通入空气,点燃酒精灯加热. | 黑色固体燃烧, |
| 乙组 | 取少量该黑色固体于a中,通入 | 黑色固体剧烈燃烧,发出白光,b中溶液变浑浊. |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、K2CO3 |
| B、BaCl2 |
| C、H2SO4 |
| D、Na2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
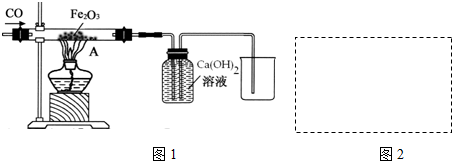
| 物质性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com