
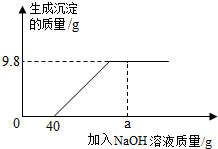
 现有含HCl和CuCl2的混合溶液65.3g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示.
现有含HCl和CuCl2的混合溶液65.3g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示.分析 稀盐酸和氢氧化钠反应生成氯化钠和水,氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,根据图中提供的信息和反应的化学方程式可以进行相关方面的计算和判断.
解答 解:(1)当加入NaOH溶液质量为ag时,溶液中的溶质有反应生成的氯化钠和过量的氢氧化钠.
故填:氯化钠、氢氧化钠.
(2)设混合溶液中CuCl2的质量为x,反应的氢氧化钠质量为y,生成氯化钠质量为z,
由图中信息可知反应生成氢氧化铜的质量是9.8g,
CuCl2+2NaOH═Cu(OH)2↓+2NaCl,
135 80 98 117
x y 9.8g z
$\frac{135}{x}$=$\frac{80}{y}$=$\frac{98}{9.8g}$=$\frac{117}{z}$,
x=13.5g,y=8g,z=11.7g,
答:混合溶液中CuCl2的质量是13.5g.
(3)设稀盐酸和氢氧化钠反应生成氯化钠的质量为m,
由图中可知和稀盐酸反应的氢氧化钠溶液质量是40g,
NaOH+HCl═NaCl+H2O,
40 58.5
40g×10% m
$\frac{40}{40g×10%}$=$\frac{58.5}{m}$,
m=5.85g,
恰好完全反应时和氯化铜反应的氢氧化钠溶液质量为:8g÷10%=80g,
恰好完全反应时,所得溶液中溶质的质量分数为:$\frac{11.7g+5.85g}{63.5g+40g+80g-9.8g}$×100%=10.1%,
答:恰好完全反应时,所得溶液中溶质的质量分数为10.1%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 银水银Ag | B. | 碳酸钠纯碱Na2CO3 | ||
| C. | 氧化钙生石灰CaO | D. | 氢氧化钠苛性钠NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
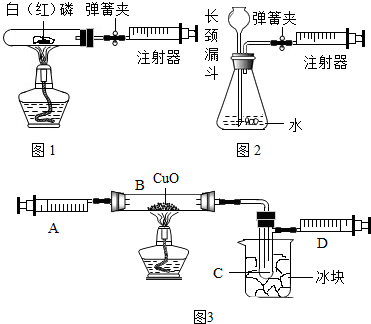 注射器是一种普通的医疗器械,但它在化学实验装置中出现的越来越多,它对某些实验现象的观察或实验过程的改进,起到了意想不到的效果
注射器是一种普通的医疗器械,但它在化学实验装置中出现的越来越多,它对某些实验现象的观察或实验过程的改进,起到了意想不到的效果查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
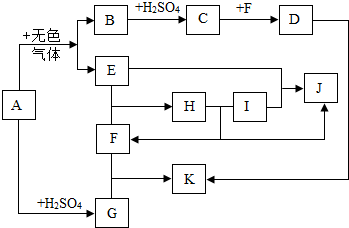 A~K是初中化学的常见物质,相互转化关系如下图所示,其中A为红棕色固体,F俗称烧碱,在工业上的用途常用于造纸、纺织,J为大理石的主要成分,沉淀D不稳定,在空气中会迅速和O2、H2O反应得到沉淀K.
A~K是初中化学的常见物质,相互转化关系如下图所示,其中A为红棕色固体,F俗称烧碱,在工业上的用途常用于造纸、纺织,J为大理石的主要成分,沉淀D不稳定,在空气中会迅速和O2、H2O反应得到沉淀K.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 验证内容 | 操作要点 | 实验现象 | 结论 |
猜想① |  向盛满二氧化碳的集气瓶中撒入足量的过氧化钠粉末,充分振荡,并将带火星的木条伸入集气瓶中 | 带火星的木条复燃 | 猜想①成立 |
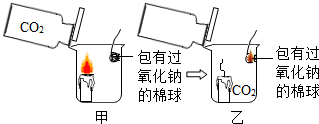
猜想② | 用如图所示装置进行实验, 点燃蜡烛,放置足够长 (比魔术所用时间更长)时间 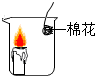 | 无现象 | 猜想②不成立 |
猜想③ | (根据你的猜想设计实验验证)向盛满二氧化碳的集气瓶中加入适量二氧化碳,用手触摸瓶壁 | 瓶壁温度升高 | 猜想③成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com