
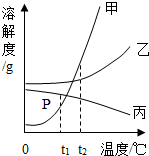
 如图为甲、乙、丙三种固体物质的溶解度曲线,请回答相关问题:
如图为甲、乙、丙三种固体物质的溶解度曲线,请回答相关问题:分析 (1)交点表示该温度下两种物质的溶解度相等;(2)根据t2℃时甲、乙、丙三种物质的溶解度大小考虑,溶解度大需要的溶剂质量小;(3)不饱和溶液变为饱和溶液的方法:加入溶质、蒸发溶剂、改变温度;(4)根据将t1℃甲、乙、丙三种物质的饱和溶液分别升温到t2℃,溶解度的变化考虑.
解答 解:(1)交点表示该温度下两种物质的溶解度相等,所以交点P点的含义是t1℃时甲和丙的溶解度相同;
(2)t2℃时甲、乙、丙三种物质的溶解度大小是:甲>乙>丙,溶解度大需要的溶剂质量小,所以所需溶剂的质量的关系是:丙>乙>甲;
(3)不饱和溶液变为饱和溶液的方法:加入溶质、蒸发溶剂、改变温度,所以t2℃将接近饱和的丙溶液变饱和的方法是加入丙或蒸发水或升高温度;(4)t1℃甲、乙、丙三种物质的饱和溶液溶质质量的分数大小是:乙>丙>甲,分别升温到t2℃时,甲和乙的溶解度变大,溶液由饱和变为不饱和,溶质质量分数不变,升温后还是乙>甲,丙升温后溶解度变小,析出晶体,溶质质量分数变小,且升温后的溶解度小于甲升温前的溶解度,所以升温后溶质质量分数大小关系是:乙>甲>丙.
故答案为:(1)t1℃时甲和丙的溶解度相同.(2)丙>乙>甲(3)加入丙(或升高温度或蒸发水)(4)乙
点评 溶解度曲线上的点属于饱和溶液,在溶解度曲线上的点不管是升温还是降温,只要向着溶解度增大的方向移动,就会由饱和变为不饱和,不会析出晶体,溶质质量分数不变;只要向着溶解度减小的方向移动,会析出晶体,溶质质量分数变小.


 习题精选系列答案
习题精选系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 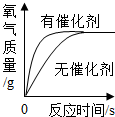 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 | |
| B. | 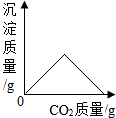 表示澄清石灰水中持续通入CO2 表示澄清石灰水中持续通入CO2 | |
| C. | 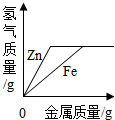 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 | |
| D. | 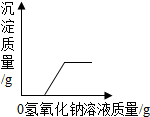 向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液 向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算:某纯碱样品中含有少量氯化钠.为测定样品中碳酸钠的质量分数,现称取该样品11.0g,放入烧杯中加水完全溶解后滴加上述配制的盐酸溶液至完全反应,最后测得生成气体的质量为4.4g,计算:
如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算:某纯碱样品中含有少量氯化钠.为测定样品中碳酸钠的质量分数,现称取该样品11.0g,放入烧杯中加水完全溶解后滴加上述配制的盐酸溶液至完全反应,最后测得生成气体的质量为4.4g,计算:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁与稀盐酸反应:2Fe+6HCl═2FeCl3+3H2↑ | |
| B. | 铁丝在氧气中燃烧:3Fe+2O2═Fe3O4 | |
| C. | 利用一氧化碳的还原性冶炼金属:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$ Cu+CO2 | |
| D. | 食盐溶于硝酸钾溶液:NaCl+KNO3═NaNO3+KCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com