
【题目】现有氧化铜和铜的混合物,对其成分进行分析.取24g此样品,向其中加入稀硫酸200克,使之充分反应.每次所用稀硫酸的质量及剩余固体的质量记录于下表:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量/g | 50 | 50 | 50 | 50 |
充分反应后剩余固体质量/g | 16 | 8 | 4 | m |
试回答下列问题:
(1)上述表格中m的值为___________,24g样品中CuO的质量为______________g.
(2)计算所加入稀硫酸的溶质的质量分数为_______?
(3)请在画出在24克样品中加入稀硫酸的质量与消耗氧化铜质量变化关系示意图_________?

【答案】4 20 19.6% 
【解析】
(1)氧化铜和铜的混合物,取24g此样品,向其中加入稀硫酸200克,只有氧化铜与稀硫酸发生反应:第一次加入50g稀硫酸,消耗氧化铜的质量=24g-16g=8g;第二次加入50g稀硫酸,消耗氧化铜的质量=16g-8g=8g;第三次加入50g稀硫酸,消耗氧化铜的质量=8g-4g=4g,说明氧化铜反应完全,剩余的4g为铜的质量;故第四次加入稀硫酸,剩余固体质量仍然为铜的质量4g,m的值为4;24g样品中CuO的质量为20g;
(2)设消耗稀硫酸的质量为x,

80/20g=98/x,x=24.5g
由(1)可知,第三次的稀硫酸只反应了25g,一共消耗稀硫酸125g,稀硫酸的溶质的质量分数=![]() ;
;
(3)24克样品中加入稀硫酸的质量与消耗氧化铜,每加入25g稀硫酸,消耗氧化铜4g,故质量变化为:


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:初中化学 来源: 题型:
【题目】(1)小明同学去黄山旅游时,用瓶装了一些山下的泉水,带回实验室在老师的指导下,按下列流程进行实验,制取蒸馏水。请回答下列问题:
①进行过滤操作时,下列做法错误的是______________(填 字母序号)
A.玻璃棒靠在滤纸连缘的任一下方
B.漏斗下端的管口管口要紧靠烧杯的内壁
C.滤纸的边缘要低于漏斗口
D.液面要低于滤纸边缘
②向滤液中加入活性炭,利用其__________性,除去水样中的色素和异味。
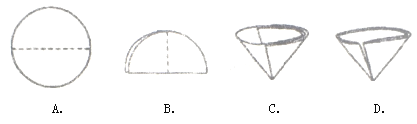
③在过滤操作中需要将圆形滤纸折叠处理,下图中不该出现的情形是 _____(填字母序号)。
(2)某同学用高锰酸钾制取氧气的实验过程如下:

①选择适当仪器,组装成如上图所示的实验装置;
②检查装置气密性,装置气密性良好;
③向集气瓶中加水,并倒置于盛有水的水槽中,集气瓶底部出现气泡;
④将药品平铺于干燥试管底部,在导管口放置蓬松的棉花团,塞上橡皮塞,固定于铁架台上;
⑤点燃酒精灯加热,待导管口有气泡产生,立即用集气瓶进行收集;
⑥气体收集完毕,用毛玻璃片将集气瓶口盖好,从水中取出并正放在桌面上;
⑦先熄灭酒精灯,后将导管从水槽中取出:
请回答下列问题:
a.用高锰酸钾制氧气所发生的化学反应的类型属于 ______;
b.步骤④中在导管口放置一小团棉花的原因是_________;
C.上述实验步骤中,可能导致集气瓶中收集的氧气不纯净(水蒸气不计)的是____(填步骤序号);
d.步骤⑦中的操作,可能导致的后果是 _________________。
f.若加热31.6克高锰酸钾使其完全分解,可生成氧气________克?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图A、B、C是三个与磷燃烧有关的实验.下列说法错误的是( )

A. 实验一的目的是探究空气中氧气的含量
B. 实验二中,既可利用玻璃管引燃红磷,又可用气球缓冲瓶内压力
C. 实验三中,采用了对比实验的研究方法,②③对比说明物质燃烧需要氧气
D. 实验三中,采用了对比实验的研究方法,①②对比说明两物质的着火点不同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动,请你和他们仪器完成以下实验探究。
(1)(演示实验)将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中,该反应的化学方程式是_____________(查阅资料)CaCl2溶液显中性
(提出问题)实验中未观察到明显显像,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
(2)(猜想与假设)针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl2 猜想Ⅱ:有_____________;猜想Ⅲ:有CaCl2和Ca(OH)2;猜想Ⅳ:有CaCl2、HCl和Ca(OH)2
(3)乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是_______________
(4)(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
实验方案 | 滴加紫色石蕊溶液 | 通入 | 滴加 |
实验操作 |
|
|
|
实验现象 | ________________ | ________________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出结论)通过探究,全班同学一致确定猜想Ⅲ是正确的。
(5)(评价反思)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因_______________________________
(6)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑______________
(7)若用200克稀盐酸和12克石灰石(杂质不溶于水也不溶于酸)反应制取二氧化碳气体为4.4克,则该石灰石中CaCO3质量分数是多少?________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是钠元素、氯元素在元素周期表中的信息及有关粒子的结构示意图。请回答下列问题:

(1)A图表示的粒子是______________(写化学符号),氯原子的核外电子数是________;
(2)钠元素与氯元素在元素周期表中处于同一周期的原因是___________;
(3)与元素的化学性质关系最密切的是______________(填序号)。
①原子的核外电子数 ②元素的相对原子质量 ③元素的质子数 ④原子的最外层电子数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料一直被广泛运用。请思考并回答下列有关金属的问题:
(1)铁能压成铁片,是利用了铁的_____性。
(2)目前工业冶炼铝的原理是:在熔融状态下电解氧化铝,生成铝和氧气。请写出该反应的化学方程式_____。
(3)为了验证铁、铜、银的金属活动性强弱,小张按照下图所示步骤进行实验(药品提供如下),且每步实验均有明显现象。请将实验步骤、现象及其有关结论填写在相应的空格中。实验室可供使用的药品(金属均提前用砂纸打磨):铁丝、铜丝、银丝、硝酸亚铁溶液、硝酸铜溶液、硝酸银溶液。
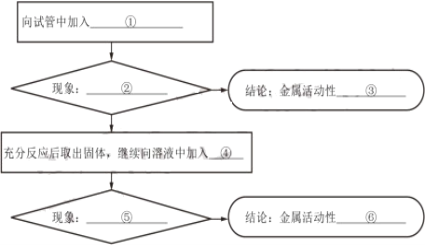
①_____②_____③_____④_____⑤_____⑥_____。
(4)早在春秋战国时期,我国就开始生产和使用铁器。目前工业炼铁的原理是在高炉中利用炉内反应生成的一氧化碳将铁从铁矿石中还原出来。请利用化学方程式进行如下计算:用800t 含氧化铁 72%的赤铁矿石,理论上可以炼出含铁 90%的生铁的质量是多少?_____(写出完整计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)用化学用语填空
①铝元素_____
②氦气_____
③2个二氧化氮分子_____
④镁离子_____
⑤硝酸根离子_____
⑥标出KClO3中氯元素的化合价_____
(2)写出下列数字意义:
①2CH4中“4”的含义_____
②2NH4+中“2”的含义_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A,B.C、D.E为初中化学常见物质,其中C为世界上年产量最大的金属,它们之间的转化关系如图所示(反应条件,部分反应物和生成物已路去)

(1)反应①的化学方程式为________
(2)反应②的化学方程式为__________
(3)E物质的化学式为_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com