
���� ��1�����ݲ��ϵķ������������
��2���ڽ������˳���У���ǰ�Ľ��������ᷴӦ����������λ����ǰ�Ľ����ܽ�λ�����Ľ�����������Һ���û��������ݴ˿��ԱȽϽ����Ļ��˳��
��� �⣺
��1���ٸ������ںϽ����ڽ������ϣ��ڵ����Ǻϳ���ά�������л��ϳɲ��ϣ�
��2���������֪���Һͱ�ͬʱ����ϡ�����У����ҵı�������������ݣ����ı���û������˵�����ҵĻ�Դ��ڱ�����������Ȼ�������Ե�����ʽ���ڣ�˵���Ļ�ѧ���ʲ����ã��ۺ����Ϸ�����֪�����ֽ����Ļ�ԵĴ�С�ǣ��ң������ף�
��������ϡ�����еķ�Ӧ��������ϡ���ᷴӦ����ѧ��Ӧ����ʽΪ��Fe+2HCl=FeCl2+H2����
�𰸣�
��1����A����B��
��2���ң������ף�Fe+2HCl=FeCl2+H2����
���� ���⿼�������������������������صĻ�ѧ֪ʶ���ѶȲ���ͬѧ��Ҫ�����ý����˳������ʵ�飬ȥ��֤�����Ļ�ԭ��ǿ����ǰ�ߵĽ�����Ѻ�ߵĽ�����������Һ���û�������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 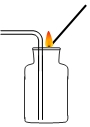 ���������̼�Ƿ��� | B�� | 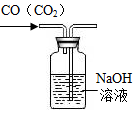 ��ȥCO�е�CO2 | ||
| C�� |  �ռ�һƿ������̼ | D�� | 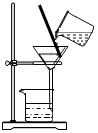 ������Һ�еĹ�̬���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 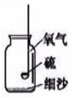 ����������ȼ�� | B�� |  ��֤�����غ㶨�� | ||
| C�� |  ��֤��ѧ��Ӧ���������仯 | D�� |  �ռ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
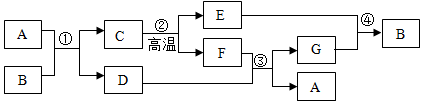
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ����ˮ��ʹ��������ԭ����ˮ�����������࣬�����¯��ˮ���� ������һ�����������ߵ�ϲ�����䲻�����Ǽ������ֱ�����ϴ����������ڣ�������
����ˮ��ʹ��������ԭ����ˮ�����������࣬�����¯��ˮ���� ������һ�����������ߵ�ϲ�����䲻�����Ǽ������ֱ�����ϴ����������ڣ�������| A�� | �ϳɲ��� | B�� | �Ͻ� | C�� | ������ | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��һ | ���� | ||||||
| �������� | ������������ָ�� ��AQI�� | ״�� | ��Ҫ��Ⱦ�� | ���� ���� | ��ƽ��Ũ�� ����/�����ף� | ��ָ�� ��IAQI�� | |
| ���� | 101 | III1 ������Ⱦ�� | ����������� | ���� | 89 | 118 | |
| ���� | 96 | II ������ | ����������� | ���� | 72 | 97 | |
| ���� | 83 | II ������ | ����������� | ���� | 60 | 82 | |
| ���� | 92 | II ������ | ����������� | ���� | 105 | 138 | |
| ���� | 91 | II ������ | ����������� | ���� | 50 | 69 | |
| ���� | 124 | III1 ������Ⱦ�� | ����������� | ���� | 101 | 133 | |
| ��ɽ | 73 | II ������ | ����������� | ��ɽ | 37 | 53 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N2 | B�� | N2O | C�� | NO | D�� | NO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com