
| 18g |
| 18g+50g |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:
 甲烷是天燃气的主要成分,其分子结构如图所示,下列关于甲烷的叙述不正确的是( )
甲烷是天燃气的主要成分,其分子结构如图所示,下列关于甲烷的叙述不正确的是( )| A、甲烷由碳、氢元素组成 |
| B、甲烷分子中碳、氢原子个数比为1:4 |
| C、一个甲烷分子中中子总数是10 |
| D、甲烷属于有机化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 元素名称 | 碳 | 氧 | 硫 | 氯 | 钠 | 钙 |
| 元素符号 | C | O | S | Cl | Na | Ca |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
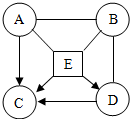 已知A、B、C、D、E均为初中化学常见的酸、碱、盐.其中A为胃酸的主要成分,B是碱,C是生理盐水的组成成分,E在工业上广泛的应用于玻璃、造纸等的生产.将它们配成溶液后,存在如右图所示的转化关系,已知A和E能反应产生气体,请回答下列问题.(“-”表示相互间能反应,“→”表示在某种条件下能生成该物质)
已知A、B、C、D、E均为初中化学常见的酸、碱、盐.其中A为胃酸的主要成分,B是碱,C是生理盐水的组成成分,E在工业上广泛的应用于玻璃、造纸等的生产.将它们配成溶液后,存在如右图所示的转化关系,已知A和E能反应产生气体,请回答下列问题.(“-”表示相互间能反应,“→”表示在某种条件下能生成该物质) 查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
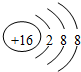 ,则下列说法不正确的是( )
,则下列说法不正确的是( )| A、该元素是一种非金属元素 |
| B、该微粒是带两个单位负电荷的阴离子 |
| C、该微粒的质子数是18 |
| D、该微粒的原子核外有18个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com