
分析 (1)根据促进化学反应速率的方法来分析;
(2)分析步骤②为过滤操作;
(3)根据反应的原理来分析解答.
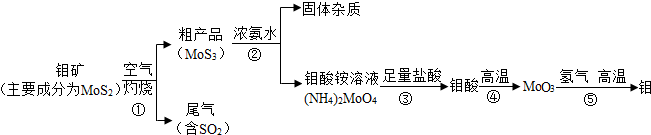
解答 解:(1)步骤①中,灼烧钼矿通常会将矿石粉碎成小颗粒,其目的是增大与氧气的接触面积,使反应更充分,提高钼矿利用率;故填:增大与氧气的接触面积,使反应更充分,提高钼矿利用率;
(2)过滤操作中需要用到的玻璃仪器有烧杯、漏斗、玻璃棒;故填:ABC;
(3)步骤⑤是氢气在高温的条件下将金属氧化物还原为金属单质,同时生成了水;故填:MoO3+3H2 $\frac{\underline{\;高温\;}}{\;}$ Mo+3H2O.
点评 本题考查物质分离和提纯,为高频考点,侧重考查学生分析计算能力,明确每一步发生的反应、操作方法是解本题关键.


 字词句段篇系列答案
字词句段篇系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用玻璃棒蘸取少量待测液滴在湿润的pH试纸上,与标准比色卡对照并读出pH | |
| B. | 收集氧气时,将带火星木条放到集气瓶口,若木条复燃,证明瓶内已集满氧气 | |
| C. | 向鸡蛋清中滴加几滴浓硝酸,微热,出现黄色 | |
| D. | 将碘水滴加在馒头片上,出现蓝色 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验装置 | 实验现象 | 实验结论 |
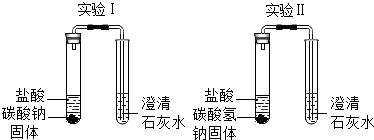 | 实验Ⅰ、Ⅱ中均观察到:白色固体逐渐减少,有气泡产生;澄清石灰水变浑浊 | Na2CO3和NaHCO3都能与盐酸反应产生CO2;NaHCO3与盐酸反应的化学方程式是NaHCO3+HCl═NaCl+H2O+CO2↑ |
| t1/℃ | t2/℃ | t3/℃ | |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
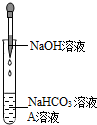
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅰ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 | 澄清石灰水无明显变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 准备食材制作粽子.
准备食材制作粽子.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 淡水资源是取之不尽、用之不竭的 | |
| B. | 水电解所生成氢气和氧气的质量比为2:1 | |
| C. | 海水、湖水是混合物,自来水是纯净物 | |
| D. | 蒸馏可使海水转化为软水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
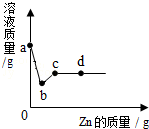 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如右图所示,关于反应有下列说法:
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如右图所示,关于反应有下列说法:| A. | ①②⑤⑦ | B. | ①③⑤⑦ | C. | ②③⑤⑦ | D. | ②④⑥⑦ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 排水法收集气体时,集气瓶中的水 | |
| B. | 加热试管内液体时,试管内的液体试剂 | |
| C. | 蒸发时,蒸发皿中的溶液 | |
| D. | 加热时,酒精灯中的酒精 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com