
| 物 质 | A | B | C | D |
| 反应前质量/g | 19.7 | 8.7 | 21.6 | 0.4 |
| 反应后质量/g | 待测 | 17.4 | 0 | 3.6 |
| A. | 物质C一定是化合物,物质D可能是单质 | |
| B. | 反应后密闭容器中A的质量为19.7g | |
| C. | 反应过程中,物质B和物质D变化的质量比为87:36 | |
| D. | 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1 |
分析 根据质量守恒定律,可分析先B、C、D三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定A是反应物还是生成物,进而根据题中数据结合各选项分析即可.
解答 解:由表中数据分析可知,反应前后,B的质量增加了8.7g,故B是生成物,参加反应的B的质量为8.7g;同理可以确定C是反应物,参加反应的C的质量为21.6g;D的质量增加了3.2g,故D是生成物,参加反应的D的质量为3.2g;由质量守恒定律,A应是生应物,且生成的A的质量为21.6g-8.7g-3.2g=9.7g.
A、该反应的反应物为C,生成物是A、B、D,因此物质C一定是化合物,物质D可能是单质,故选项说法正确.
B、生成的A的质量为9.7g,则待测的值为9.7g+19.7g=29.4g,故选项说法错误.
C、由质量守恒定律,物质B和物质D质量增加的比为(17.4g-8.7g):(3.6g-0.4g)=87:32,故选项说法错误.
D、A增加的质量是9.7g,C减小的质量是21.6g,因为物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为$\frac{9.7}{194}$:$\frac{21.6}{216}$=1:2;
故选:A.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据、灵活运用质量守恒定律.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 农业上用氯化钠溶液选种 | |
| B. | 生活中用活性炭除去房间中的甲醛 | |
| C. | 农业上用二氧化碳作温室中气体肥料 | |
| D. | 生活中用大理石作装饰材料 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
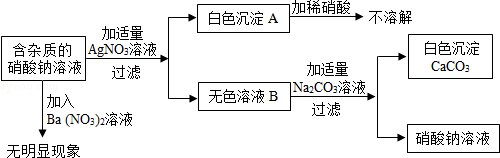
| A. | 无色溶液B的溶质是硝酸钙 | |
| B. | 原溶液中的杂质只有氯化钙 | |
| C. | 原溶液中的杂质可能由氯化钙、硝酸钙和氯化钠三种物质组成 | |
| D. | 该实验中涉及的基本反应类型不止一种 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
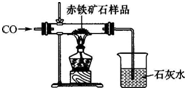 (1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)
(1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)| 反应前 | 氧化铁完全反应后 | |
| A组 | 玻璃管和赤铁矿石样品的质量m1g | 玻璃管和固体物质的质量m2g |
| B组 | 烧杯和澄清石灰水的质量m3g | 烧杯和烧杯中物质的质量m4g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
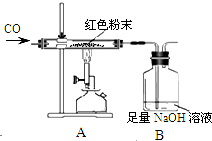 某化学兴趣小组对一包干燥的红色粉末组成进行探究,同学们根据该红色粉末的来源,判断其可能由Cu、Fe2O3两种固体中的一种或两种组成.
某化学兴趣小组对一包干燥的红色粉末组成进行探究,同学们根据该红色粉末的来源,判断其可能由Cu、Fe2O3两种固体中的一种或两种组成.| 反应前 | 反应后 | |
| Ⅰ组 | 玻璃管和红色粉末的总质量为48.3g | 玻璃管和固体物质的总质量为47.1g |
| Ⅱ组 | 洗气瓶和瓶中所盛物质的总质量为258.6g | 洗气瓶和瓶中所盛物质的总质量为261.9g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com