
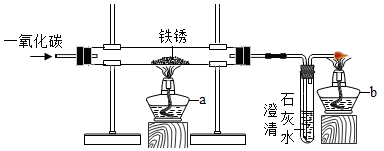
分析 根据已有的铁生锈的知识进行分析解答,铁在与水和氧气并存时易生锈.根据一氧化碳有毒,直接排放会污染空气来分析解答;
【实验操作】根据一氧化碳的可燃性分析;
【现象分析】根据一氧化碳还原氧化铁的现象来分析;
【实验设计】根据金属的性质来分析;
【实验反思】一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间,从而考虑装置的改进;
【重新实验】根据金属的化学性质来分析;
【拓展应用】根据减少的质量为氧化铁中氧元素的质量以及化学方程式来分析.
解答 解:铁在与水和氧气并存时易生锈,故填:氧气、水蒸气(或O2、H2O)
如果通入的CO过量,有毒的一氧化碳就会沿导管排入大气中,所以尾气要处理后排入大气.用酒精灯将其点燃,是为了防止造成空气的污染,故填:点燃多余的一氧化碳,防止污染空气;
【实验操作】一氧化碳具有可燃性,如果不纯可能发生爆炸,实验开始时,要先通一氧化碳,排净装置中的空气,防止爆炸.故填:排净装置中的空气,防止爆炸;
【现象分析】氧化铁在一氧化碳的还原作用下,由红色氧化铁粉末逐渐变成黑色铁粉末;除生成铁以外,还生成二氧化碳气体,二氧化碳与澄清石灰水反应,使澄清石灰水变浑浊,一氧化碳与氧化铁在高温的条件下,生成铁和二氧化碳,配平即可.化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.故填:红色粉末逐渐变黑;3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
【实验设计】铁能与酸反应生成氢气,所以若有铁存在,会看到有气泡产生,故填:有气泡产生;
【实验反思】一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.上图所示实验装置中,应作的一处修改是将酒精灯a换成酒精喷灯.
故填:将酒精灯a换成酒精喷灯(或给酒精灯a加网罩);
【重新实验】除上述方案,还可以采取另一种实验方案,所用的试剂是硫酸铜溶液,铁与硫酸铜反应生成铜和硫酸亚铁;所以,可通过观察是否有红色固体生成,判断黑色固体中是否含金属铁;故填:有红色固体析出;
【拓展应用】玻璃管中固体减少的质量即为氧化铁中铁元素的质量:70.0g-67.6g=2.4g;
设氧化铁的质量为x,则
3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2?固体质量减少
160 112 160-112=48
x 2.4g
$\frac{160}{x}=\frac{48}{2.4g}$
x=8.0g
该赤铁矿中氧化铁的质量分数为$\frac{8.0g}{70.0g-60.0g}×100%$=80%
故填:80%.
点评 本题综合性较强,较全面的考查了一氧化碳还原氧化铁,尤其是利用数据对混合物的判断增加了试题难度,掌握反应前后元素的质量不变,并会结合方程式分析即可顺利解答.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量反应后的溶液于试管中,滴加酚酞溶液. | 溶液不变红色. | 猜想Ⅲ不正确. |
| ②再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钙. | 有气泡产生. | 猜想Ⅰ不正确. 猜想Ⅱ正确. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com