
下图是碱式碳酸铜受热分解发生分解反应的装置图,依据图回答问题。

(1)实验时可看到绿色的碱式碳酸铜逐渐变为_____色的物质,澄清的石灰水变_____。
(2)实验结束时应先撤_____后撤_____(填摰脊軘或摼凭?茢)。理由是______________________________。
(3)实验室还可以用此反应装置制取_____气,反应的化学方程式是______________________________。
(4)若保持反应装置中试管口稍向下倾斜不变,稍作其他改动,做加热高锰酸钾制氧气的实验,则必须在试管口_____,若做氢气还原氧化铜的实验,除了去掉橡皮塞外,还必须把通氢气的导管伸入_____。
科目:初中化学 来源: 题型:
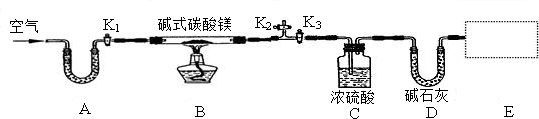
| 反应前 | 反应后 |
| C装置及药品总质量:87,6g | C装置及药品总质量:89,4g |
| D装置及药品总质量:74,7g | D装置及药品总质量:83,5g |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| △ |
| ||
| △ |
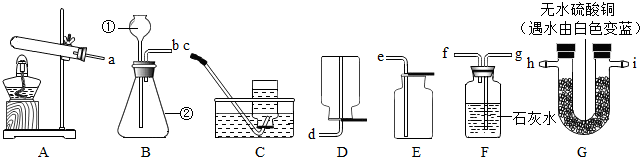
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
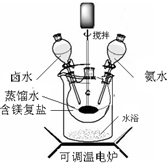 碱式碳酸镁密度小,是橡胶制品的优良填料.其组成一般以xMgCO3?yMg(OH)2?zH2O表示.
碱式碳酸镁密度小,是橡胶制品的优良填料.其组成一般以xMgCO3?yMg(OH)2?zH2O表示.| 实验操作 | 实验现象 | 实验结论 |
| ①取样溶解,向样品溶液中滴加过量稀硝酸. ②再向上述所得溶液加 硝酸银或AgNO3 硝酸银或AgNO3 溶液 |
现象① 产生气泡 产生气泡 ;现象② 产生白色沉淀 产生白色沉淀 ; |
含有 Cl- |
| ||
查看答案和解析>>
科目:初中化学 来源:专项题 题型:实验题
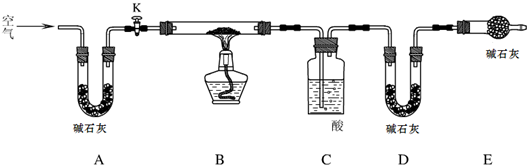
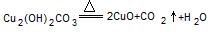 ,某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比。
,某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比。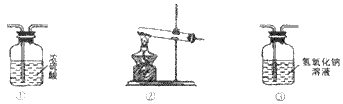
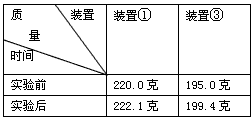
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com