
N2O 俗称“笑气”,具有麻醉作用。在 N2O 中,氮元素的化合价为( )
A. -1 B. - 2 C. + 1 D. + 2
C 【解析】在 N2O 中,氧元素显-2价,设:氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(-2)=0,则x=+1。故选C。 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:初中化学 来源:辽宁大连汇文中学2018年期中模拟化学试卷 题型:填空题
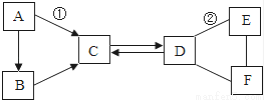
A~F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“﹣”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去)
请回答:
(1)E的化学式________ ;C的化学式________ .
(2)写出有关反应的化学方程式:①________ ;②________ .
查看答案和解析>>
科目:初中化学 来源:临沂市2018年九年级化学中考模拟试卷 题型:单选题
甲、乙两种物质的溶解度曲线如图所示,下列叙述错误的是( )
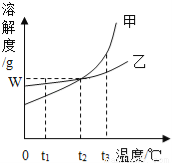
A. t1℃时,甲的溶解度小于乙的溶解度
B. t1℃时,加入甲物质,可使不饱和的甲溶液变成饱和
C. t2℃时,甲或乙两种物质饱和溶液中溶质与溶剂的比是W:100
D. 将甲、乙饱和溶液的温度从t3℃降到t2℃时,乙先析出晶体
D 【解析】试题分析:溶解度曲线意义:1、表示某物质在不同温度下的溶解度或溶解度随温度变化的情况,进而判断结晶的方法,①溶解度随温度的升高而增大,采用冷却热饱和溶液(即降温结晶),②溶解度随温度的升高而变化不大,采用蒸发结晶,2、两曲线的交点表示两种溶质在同一温度下具有相同的溶解度,3、可比较同温下,不同物质溶解度的大小关系,4、可直接读出某温下,物质的溶解度; A、t1℃时,甲的溶解度小于...查看答案和解析>>
科目:初中化学 来源:云南省昆明市业水平考试化学试卷 题型:简答题
金属材料与人类的生产生活密切相关。
(1)下列主要利用了金属导热性的是 ___。
A. 铁做炊具 B. 铜做导线 C. 铝制成铝箔
(2)在铁的表面喷漆或涂油可有效防止铁生锈,原因是 ________ ;在喷漆或 涂油前通常要进行基面清理,其中最主要的就是除去铁锈,请写出用稀盐酸除去铁锈的化学反应方程式 _______。
(3)将一块锌铁合金放入一定质量的 CuCl2 溶液中,充分反应后过滤,得到滤渣和滤 液,烘干滤渣进行称量,发现滤渣的质量和所加锌铁合金的质量恰好相等,则滤液中一定含有的溶质是 _______;若往滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定存有的物质是 ________。某同学为探究 Al、Cu 和 Ag 三种 金 属 的 活 动 顺 序 , 请 你 为 该 同 学 提 供 三 种 药 品 , 你 提 供 的 三 种 药 品 是____合理即可)。
A 隔绝了氧气和水; Fe2O3+6HCl=2FeCl3+3H2O ZnCl2、FeCl2 Cu、Fe Al、Cu(NO3)2、Ag 【解析】本题考查了金属的性质,金属活动性顺序探究和应用。 (1)A、铁做炊具是利用了铁的导热性,符合题意;B、铜做导线是利用了铜的导电性,不符合题意;C、铝制成铝箔是利用了铝的延展性,不符合题意。故选A; (2)在铁的表面喷漆或涂油可有效防止铁生锈...查看答案和解析>>
科目:初中化学 来源:云南省昆明市业水平考试化学试卷 题型:单选题
甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法正确的是( )
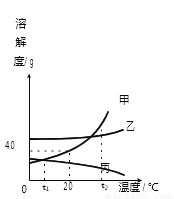
A. 甲与丙的溶解度相等
B. 20℃时,将 30g 甲放入 50g 水中,充分搅拌, 甲所得溶液的质量为70g
C. 分别将 t2℃时甲、乙的饱和溶液降温到t1℃,甲溶液中析出的晶体质量大
D. 将 t2℃时三种物质的饱和溶液降温到t1℃,溶液中溶质的质量分数:乙>甲=丙
B 【解析】A、温度没有确定不能比较两物质的溶解度,错误;B、20℃时,甲的溶解度为40g,20℃时,100g水中最多溶解40g的甲,将 30g 甲放入 50g 水中,充分搅拌,能溶解20g,所得甲溶液的质量为70g,正确;C、没有确定溶液的质量,不能比较饱和溶液降温后析出晶体的擀质量,错误;D、甲、乙的溶解度随温度降低而减小,丙的溶解度随温度降低而增大,所以分别将t2℃时三种物质的饱和溶液...查看答案和解析>>
科目:初中化学 来源:云南省昆明市业水平考试化学试卷 题型:单选题
下列有关化学与人体健康的叙述正确的是( )
A. 缺碘会引起甲状腺肿大 B. 缺铁容易引起坏血病
C. 老年缺钙易患佝偻病 D. 缺乏维生素 C 会引起夜盲症
A 【解析】A、碘是合成甲状腺激素的主要元素,缺乏或摄入过多都会患甲状腺肿大,正确;B、铁是合成血红蛋白的主要元素,缺铁会患贫血,错误;C、钙是构成骨骼和牙齿的主要成分,它使骨骼和牙齿有坚硬的结构支架,老年缺钙易患骨质疏松症,错误;D、人体内缺乏维生素A会引起夜盲症,错误。故选A。查看答案和解析>>
科目:初中化学 来源:2018年广州市荔湾区中考化学一模八校联考试卷 题型:科学探究题
新闻事件:一辆载满20t电石的挂车,行驶在途中突然燃起熊熊大火并伴有大量黑烟。事故路面上洒落了五六百米燃着的石头,这辆货车在雨中整整燃烧了一天,消防官兵对大火也束手无策,场面让人惊心动魄,同学们看到这则新闻对电石的化学性质产生了浓厚的兴趣,请你与他们一起完成下列探究活动。
【查阅资料】:电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体。常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟。
【猜想与假设】:同学们展开大胆的猜想:
(1)根据质量守恒定律,电石与水反应生成的气体可能是:氧气、氢气或乙炔(C2H2);电石与水反应生成的白色固体可能是:氧化钙、氢氧化钙或碳酸钙.
(2)同学们讨论后一致认为:白色固体不可能是氧化钙,原因是(用化学方程式表示)________。
【实验探究】进一步确定生成物的成分
实验步骤 | 实验现象 | 实验结论 |
(1)取适量电石加水反应,收集生成的气体,验纯后点燃。 | 气体燃烧,产生黄色火焰 并伴有浓烈黑烟。 | 电石与水反应产生的气体是_______。 |
(2)取适量反应后生成的固体于试管中,滴加过量_________。 | 固体溶解,_________。 | 电石与水反应产生的固体不是碳酸钙。 |
(3)取适量反应后生成的固体于试管中,加入足量的水,振荡。静置后取少量上层清液于另一试管中,并________。 | 电石与水反应产生的固体是氢氧化钙,实验步骤3的化学反应的方程式为:_____________。 |
【反思交流】载有电石的货车可以在雨中整整燃烧一天而不熄灭,说明电石与水的反应是_______________(填“吸热”,或“放热”)反应。
CaO+H2O═Ca(OH)2 乙炔 稀盐酸 通入二氧化碳/加入碳酸钠溶液(合理即可) 不产生气泡溶液变浑浊/有白色沉淀产生(合理即可) Ca(OH)2 +CO2═CaCO3↓+H2O/Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 放热 【解析】【猜想与假设】氧化钙遇到水会产生氢氧化钙,所以白色固体不可能是氧化钙,化学方程式为:CaO+H2O═Ca(OH)2;【实验探究】(1)资料...查看答案和解析>>
科目:初中化学 来源:2018年广州市荔湾区中考化学一模八校联考试卷 题型:单选题
下列关于物质的性质和用途的表述没有直接联系的是( )
选项 | 性质 | 用途 |
A | 铝有延展性 | 能制成铝箔 |
B | 碳具有可燃性 | 常用于冶炼金属 |
C | 甲烷易燃烧,且燃烧产生大量的热 | 做燃料 |
D | 醋酸能与碳酸盐反应 | 醋酸能清洁水壶中的水垢(主要成分为碳酸钙) |
A. A B. B C. C D. D
B 【解析】A、铝有延展性,可以制成铝箔,故正确;B、碳具有还原性,可以做还原剂,常用于冶炼金属,故错误;C、甲烷易燃烧,且燃烧产生大量的热,做燃料,故正确;D、醋酸能与碳酸钙反应,能清洁水壶中的水垢,故错误。故选B。查看答案和解析>>
科目:初中化学 来源:安徽省滁州市定远育才学校2018届九年级下学期期中考试化学试卷 题型:填空题
(7分)钢铁是使用最多的金属材料。
(1)下图为实验室炼铁的装置图,A中反应的化学方程式是 ;将反应后的气体通过装置B和C,收集较纯净的CO并循环使用,B中应盛放的试剂是 浓溶液。

(2)工业上可用酸清洗锈蚀的金属。将生锈的铁片和生锈的铜片[铜锈的成分Cu2(OH)2CO3]同时放入一定量盐酸中,可能发生的化学反应有:
①铜锈溶【解析】
Cu2(OH)2CO3+ 4HCl= 2CuCl2 + 3X + CO2↑,则X的化学式为 ;
②铁锈溶【解析】
化学方程式为 ;
③有金属单质生成:化学方程式为 。
(3)某化学小组欲测定一种钢样品中铁的含量,实验操作如图所示,实验结果记录如下表:

反应时间 | t0 | t1 | t2 | t3 |
烧杯和药品质量/g | 55.7 | 55.6 | 55.5 | 55.5 |
①经计算,这种钢样品中铁的含量是 % (精确到0.1%)。
②有同学提出,灼烧可使钢中的碳转化为二氧化碳,钢样品质量会减轻。但是他们将一定量的钢样品灼烧后,发现质量反而增加了,其原因是 。
(1)3CO + Fe2O3 3CO2 +2 Fe 氢氧化钠(或NaOH) (2)①H2O ② Fe2O3 + 6HCl = 2FeCl3 + 3H2O ③ CuCl2 + Fe = Cu + FeCl2 (3)①98.2% ②钢中含碳量少,所以碳减少的质量,远小于铁转化为氧化物时增加的质量 【解析】 试题分析:(1)一氧化碳还原氧化铁的反应方程式为:3CO + Fe...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com