
| A. | 32:17 | B. | 17:32 | C. | 32:34 | D. | 34:32 |
分析 根据“反应A+2B=3C+2D中中,已知C和D的相对分子质量之比为16:9”,则可假设C和D的相对分子质量分别为16a、9a,又因为16.4g A与一定量B完全反应,生成9.6g C,则可求一定量D的质量,再根据质量守恒定律求出参加反应的B的质量,根据A、B的质量比可求出反应中A和B的相对分子质量之比.
解答 解:由“反应A+2B=3C+2D中中,已知C和D的相对分子质量之比为16:9”,则可假设C和D的相对分子质量分别为16a、9a,又因为16.4g A与一定量B完全反应,生成9.6g C,设D的质量为x
A+2B=3C+2D
48a 18a
9.6g x
$\frac{48a}{18a}=\frac{9.6g}{x}$ 解得:x=3.6g,
由质量守恒定律可知,参加反应的B的质量为:9.6g+3.6g-6.4g=6.8g
设A、B的相对分子质量分别为:m、n
由方程式可知:$\frac{m}{2n}=\frac{6.4g}{6.8g}$ 所以$\frac{m}{n}$=$\frac{32}{17}$ 所以A正确.
故选A.
点评 根据质量守恒定律是指参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和;并要学会利用质量守恒定律以及化学方程式的质量关系处理问题的方法


科目:初中化学 来源: 题型:选择题
| A. | 将二氧化碳气体通入氯化钙溶液可看到碳酸钙沉淀 | |
| B. | 铁能和稀硫酸、硫酸铜溶液、氢氧化铜发生置换反应 | |
| C. | 氢氧化钠能和盐酸、硫酸钾溶液反应 | |
| D. | 借助酚酞试液可完成稀盐酸、氯化钠溶液、氢氧化钠溶液、碳酸钾溶液间的鉴别 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/克 | 5 | 10 | 15 | 20 |
| 生成CO2的质量/克 | 1.76 | 3.52 | 4.4 | M |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 22.2 g | B. | 7.4 g | C. | 14.8 g | D. | 3.7 g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | NaCl+AgNO3=AgCl↓+NaNO3 | ||
| C. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | D. | 2HCl+Cu(OH)2=CuCl2+2H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2SO4、Ba(OH)2、H2SO4 | B. | Na2CO3、AgNO3、HCl | ||
| C. | AgNO3、CaCl2、HNO3 | D. | NaOH、MgCl2、H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用稀盐酸除去铁制品表面的铁锈:2HCl+FeO═FeCl2+H2O | |
| B. | 向Na2CO3溶液中滴加澄清的石灰水:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH | |
| C. | 用铁与稀硫酸反应制取氢气:2Fe+3H2SO4═Fe 2(SO4)3+3H2↑ | |
| D. | 用点燃的方法除去二氧化碳中少量的一氧化碳:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2 CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 准确称取5克铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有50克某质量分数的硫酸溶液的烧杯中,充分反应后过滤,再向滤液中加入20%的氢氧化钠溶液,产生沉淀的质量与所加入的氢氧化钠溶液质量的关系如右图所示.试求:
准确称取5克铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有50克某质量分数的硫酸溶液的烧杯中,充分反应后过滤,再向滤液中加入20%的氢氧化钠溶液,产生沉淀的质量与所加入的氢氧化钠溶液质量的关系如右图所示.试求:查看答案和解析>>
科目:初中化学 来源: 题型:推断题
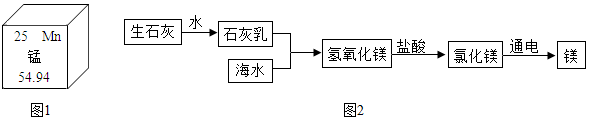
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com