
分别向
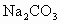 、
、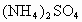 、NaCl、
、NaCl、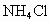 四种溶液中加入下列一种试剂,便可将它们鉴别出来,这种试剂是
四种溶液中加入下列一种试剂,便可将它们鉴别出来,这种试剂是
[
]|
A .盐酸 |
B .氯化钙溶液 |
|
C .氢氧化钠溶液 |
D .氢氧化钡溶液 |
|
解析:用一种试剂鉴别这四种溶液,必须产生四种不同的现象.在被鉴别的四种物质 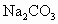 、 、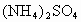 、NaCl、 、NaCl、 中,阳离子分别为 中,阳离子分别为 、 、 阴离子分别为 阴离子分别为 、 、 、 、 ,对于阳离子 ,对于阳离子 可以与碱中 可以与碱中 反应,产生有刺激性气味的 反应,产生有刺激性气味的 ,而 ,而 不与 不与 反应,所以这种试剂的组成中必须有 反应,所以这种试剂的组成中必须有 ;对于阴离子为了防止干扰可先鉴别 ;对于阴离子为了防止干扰可先鉴别 、 、 ,可用 ,可用 ,因为 ,因为 、 、 分别与 分别与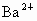 反应生成 反应生成 、 、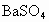 沉淀, 沉淀, 不与 不与 反应,所以这种试剂组成中必须有 反应,所以这种试剂组成中必须有 ,阴阳离子综合起来,试剂应是 ,阴阳离子综合起来,试剂应是 .将 .将 分别加入四种溶液中,产生的现象为 分别加入四种溶液中,产生的现象为 与NaCl不反应,无现象; 与NaCl不反应,无现象; 与 与 反应产生白色沉淀; 反应产生白色沉淀; 与 与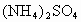 反应,既产生白色沉淀,又产生气体; 反应,既产生白色沉淀,又产生气体; 与 与 反应只产生气体,所发生反应的化学方程式分别为 反应只产生气体,所发生反应的化学方程式分别为
|
|
点拨:用一种试剂鉴别多种物质,要求这种试剂能分别跟这些物质反应产生不同的现象,鉴别时可从物质的阴、阳离子的不同点上考虑,采用分析和综合的方法思考. |


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:初中化学 来源: 题型:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 /g |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g) |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.2 |
| KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 | |
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com