
| A. | ②③ | B. | ①④ | C. | ①③ | D. | ②④ |
分析 ①根据信息素化学式的含义进行分析判断.
②根据信息素的微观构成进行分析判断.
③根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
④根据信息素的一个分子的构成进行分析判断.
解答 解:①信息素是由碳、氢、氧三种元素组成的,说法正确.
②信息素是由信息素分子构成的化合物,信息素分子是由碳、氢、氧原子构成的,说法错误.
③该信息素中碳、氢、氧三种元素的质量比为(12×10):(1×18):(16×1)≠10:18:1,说法错误.
④信息素的一个分子是由10个碳原子、18个氢原子和1个氧原子构成的,则该信息素的一个分子中含有29个原子,说法正确.
故选B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:初中化学 来源: 题型:实验探究题
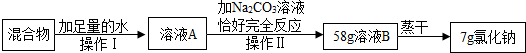
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 乙>丁>丙>甲 | B. | 甲>乙>丙>丁 | C. | 丁>丙>乙>甲 | D. | 甲>乙>丁>丙 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 江堤乐园樱花盛开时,走进园区,就能闻到淡淡地清香 | |
| B. | 50mL水与50mL的酒精混合后,体积小于100mL | |
| C. | 鼓起的篮球继续充气后,篮球的体积基本没变 | |
| D. | 水烧开后,壶盖被顶起 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
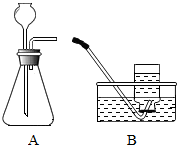 某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象:硫酸中混有硫酸铜溶液时,产生氢气的速率更快.
某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象:硫酸中混有硫酸铜溶液时,产生氢气的速率更快.| 编号 | 20%的稀硫酸各20mL | 锌粒 | 收集1瓶氢气所需的时间 |
| ① | 加入质量分数为10%的硫酸铜溶液1mL | 1g | 2分10秒 |
| ② | 加入质量分数为10%的硫酸锌溶液1mL | 1g | 3分01秒 |
| 编号 | 实验步骤 | 实验现象比较 | 实验结论 |
| ① | 取1g锌粒于锥形瓶中, 加入20mL 20%的稀硫酸 | 产生氢气的速率较快与铜单质有关 | |
| ② |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
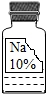 实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是NaCl、NaOH、Na2CO3、NaHCO3中的一种.小强和小华同学很感兴趣,决定对其成分进行探究:
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是NaCl、NaOH、Na2CO3、NaHCO3中的一种.小强和小华同学很感兴趣,决定对其成分进行探究:| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 盐酸(硫酸) | 产生大量的气泡 | 该溶液是Na2CO3 相关的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 盐酸的质量/g | 20 | 40 | 60 |
| 生成气体的质量/s | 2.2 | 4.4 | 5.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com